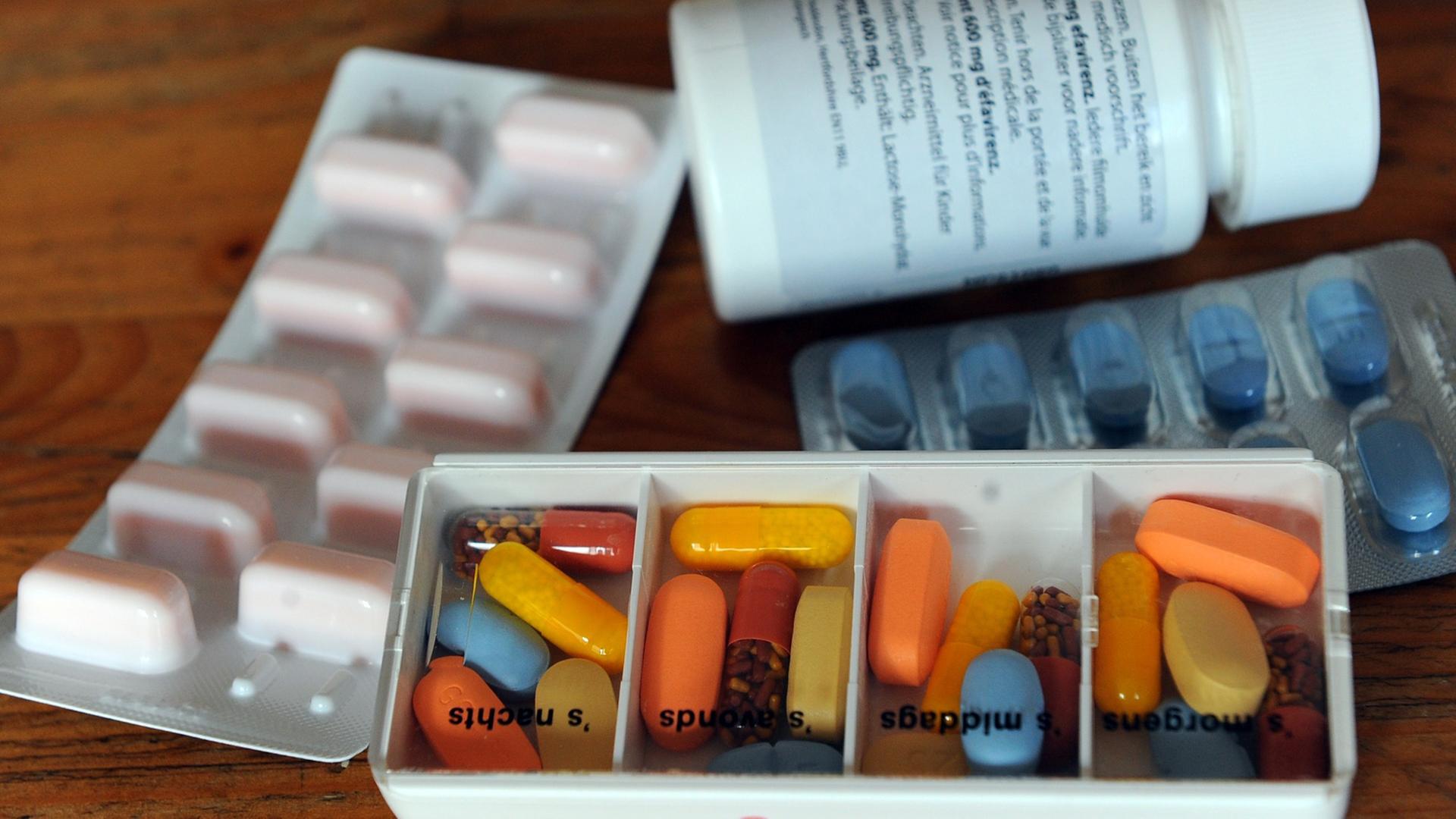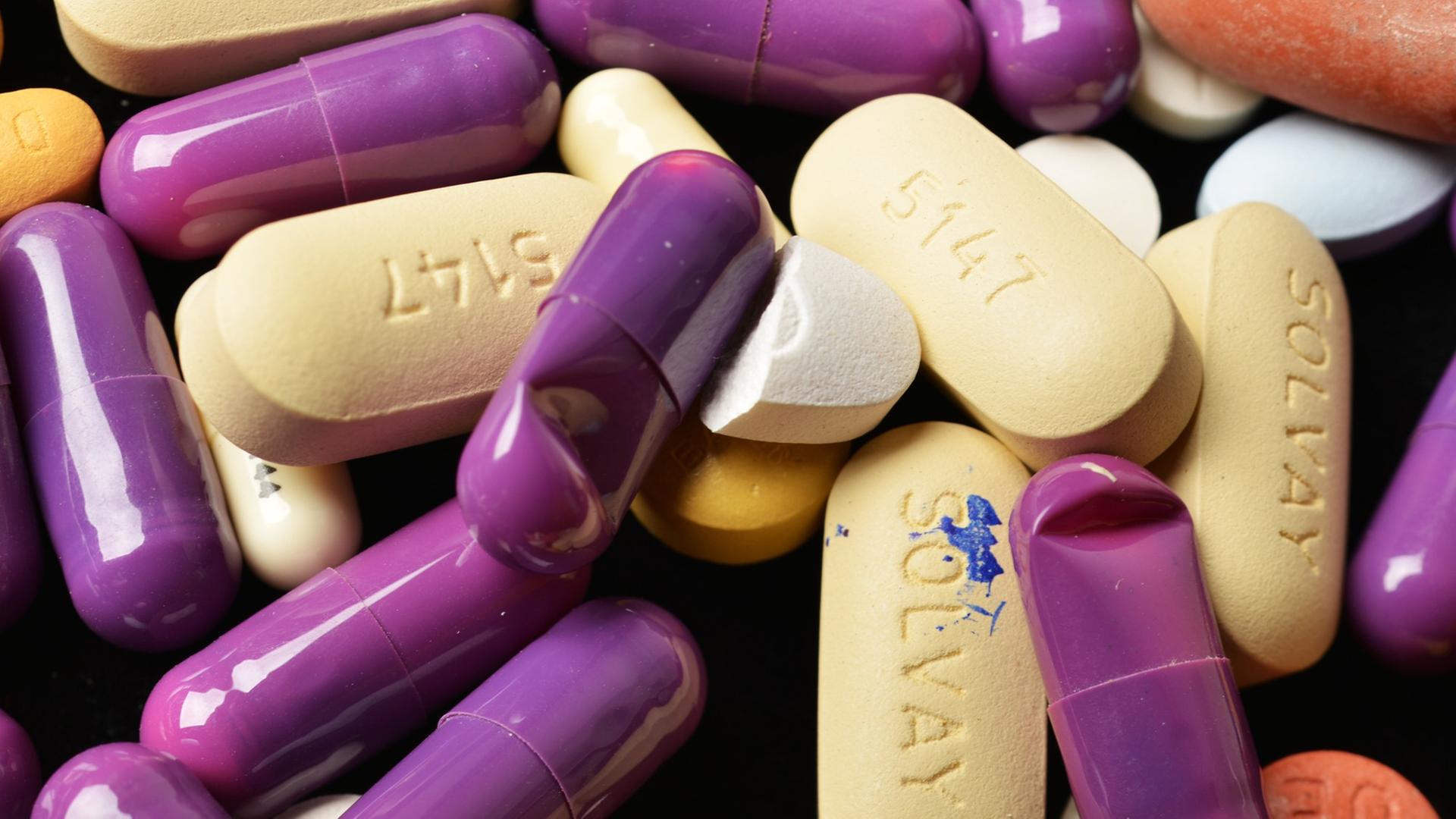
Es ist kein Geheimnis: Die präklinische Forschung pfeift auf dem letzten Mäuseloch. Hochrechnungen zufolge kommen schwindelerregende 50 bis 80 Prozent der Studien zu irreführenden Aussagen. Der Versuch, nachzuweisen, dass ein im Tierversuch erfolgreiches Medikament auch beim Menschen wirkt, scheitert deshalb oft.
Ein Problem mit vielen Ursachen, von denen mindestens eines einfach zu beheben wäre, meint Robin Kleiman. Die Neurobiologin berät am Children's Hospital in Boston Kollegen bei der Planung von präklinischen Studien. Ihrer Erfahrung nach vergessen viele Forscher, eine grundlegende Frage zu stellen: Wie hoch muss die Dosis eines Medikaments sein, damit es wirkt?
"Ich wollte einen Eindruck davon bekommen, wie groß dieses Problem tatsächlich ist. Ich habe mir also 100 Veröffentlichungen aus hochrangigen Fachjournalen vorgenommen. Das waren alle Artikel, die dort 2014 erschienen sind und gezielt die Wirkung einer Substanz im Gehirn von Mäusen untersucht haben. Ich habe geschaut, wie die Wahl der Dosis begründet wird. In einem Viertel der Arbeiten hieß es "wir verwenden Dosis X" - und das war's!"
Forscher wählen oft willkürliche Dosierungen
Um die richtige Dosis zu finden, ist es wichtig zu wissen, was mit der Substanz im Körper passiert. Wie viel davon gelangt vom Blut tatsächlich ins Gehirn? Wie groß ist der Anteil der Wirkstoffmoleküle, die auch einen Rezeptor aktivieren? Und wie viele davon werden abgebaut, bevor sie einen Effekt zeigen können? Nur fünfzehn der einhundert Studien hatten gemessen, wie viel des Medikaments überhaupt im Gehirn ankam. Und nur zwei untersuchten, wie gut der Wirkungsgrad an den Neuronen war.
"Solche pharmakokinetischen Daten sind wirklich wichtig damit andere Forscher auf den Ergebnissen einer Studie aufbauen können. Aber um diese Daten zu erheben, braucht man Wissen - und Geräte, die im Unterhalt so teuer sind, dass die meisten Unis sie sich nicht leisten können. Man kann zwar externe Firmen beauftragen aber es gibt selten Fördergelder, die für solche Zwecke vorgesehen sind. Und dann braucht man einen Experten, um die Daten zu interpretieren."
Pharmakokinetische Daten zugänglich machen
Mangels präziser Informationen setzen viele Forscher deshalb auf Versuch-und-Irrtum. Sie wählen willkürliche Dosierungen und schauen, was sie bewirken. Das Resultat sind Studien mit stark begrenzter Aussagekraft, die oft weder auf den Menschen übertragbar, noch reproduzierbar sind. Robin Kleiman hat vor ihrer Zeit an der Uni-Klinik 14 Jahre in der Industrie gearbeitet, wo pharmakokinetische Daten standardmäßig erhoben werden. Sie ist sich sicher: Ein Schulterschluss von Industrie und Hochschulen wäre für alle Beteiligten von Vorteil.
"Ich denke, es ist wichtig, solche Daten allgemein zugänglich zu machen. Sie gelten aber nicht als sonderlich innovativ und schaffen es deshalb oft nicht in die Publikationen. Würden sie in einer öffentlichen Datenbank abgelegt, könnten Forscher die Information benutzen, um die Dosierung für ihre eigene Studie passender zu wählen. Das wäre für alle gut. Auch die Industrie profitiert davon, wenn ihre potenziellen Wirkstoffe richtig dosiert werden."
Bedenken, dass gerade Industrieforscher Probleme damit haben könnten, die Wirkstoffprofile ihrer Substanzen zu teilen, hat Robin Kleiman nicht. Insbesondere bei Wirkstoffen, deren Patentschutz abgelaufen ist, wird aus den pharmakokinetischen Eigenschaften kein Staatsgeheimnis gemacht. Die Neurobiologin sieht das Problem eher darin, schlechte Angewohnheiten hinter sich zu lassen.
"Die Leute dann auch dazu zu bringen, so eine Datenbank zu füllen und zu benutzen, ist eine Herausforderung. Ich denke, die Journale werden dabei eine wichtige Rolle spielen, indem sie beim Review Prozess detailliertere Informationen zur Medikamentendosierung einfordern."
Die Bereitschaft ist da. Als Reaktion auf offensichtliche Qualitätsmängel in der Forschung haben viele Fachzeitschriften in den letzten Jahren ihre Richtlinien zur Begutachtung von Artikeln erweitert.