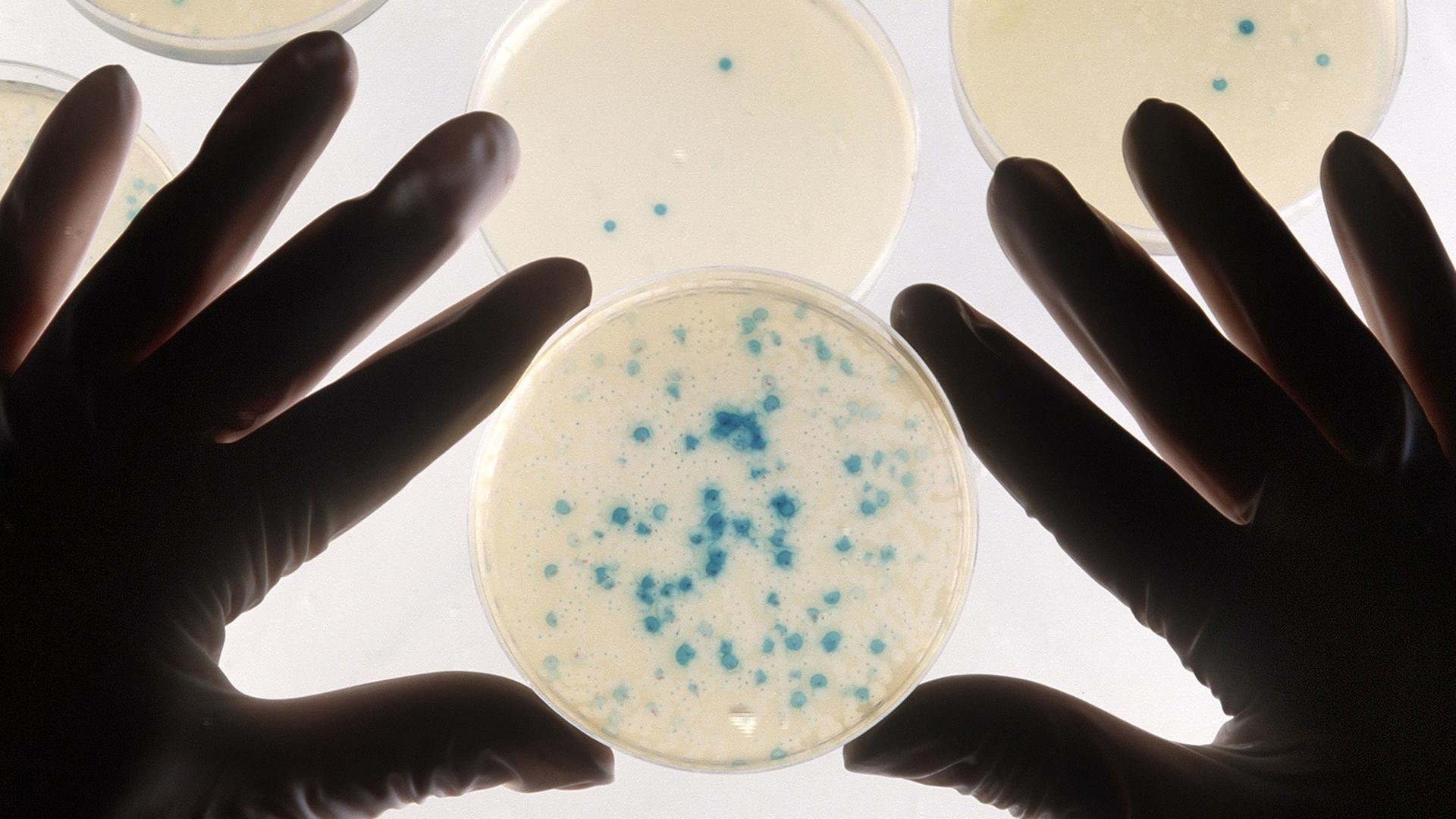
"Staphylococcus Aureus ist normalerweise gelb-golden und deshalb heißt er auch Staphylococcus Aureus, wegen der Farbe."
Gudrun Koch hält eine Petrischale in der Hand. Auf dem gelblichen Nährmedium in der Plastikschale wachsen kreisrunde Bakterienkolonie. Die goldgelben Flecken in der Mitte sind der Wildtyp des Bakteriums, um den herum sich ein Ring aus mutierten weißen Tochterzellen ausbreitet.
"Es gibt dann halt unterschiedliche Mutanten, die die Gene nicht exprimieren und darum werden die halt nicht gelb, sondern haben dann den weißen Phenotyp."
Bakterien mutieren
Gudrun Koch und ihre Kollegen am Forschungszentrum für Infektionskrankheiten der Universität Würzburg interessieren sich für die Mutanten besonders. Sie wollen wissen, wie sich Staphylococcus-Infektionen bekämpfen lassen. Deshalb suchen sie unter den Mutanten nach den Stämmen, die veränderte Eigenschaften aufweisen, also zum Beispiel einen veränderten Stoffwechsel haben. In den Kolonien treten die Mutationen immer wieder von selbst auf, denn das enge Zusammenleben in derartigen Biofilmen verändert die Zellen, wie Daniel Lopez erklärt.
"Es ist wie eine Stadt aus Mikroben. Ein kleiner Raum, auf dem Millionen und Abermillionen von Bakterien koexistieren und interagieren. Für die einzelnen Erreger können diese Interaktionen von Vorteil oder von Nachteil sein, je nachdem, wie die Bedingungen sind und welche Stämme in der Stadt zusammenleben."
Stämme können resistent werden
Sind die Bedingungen schlecht, entsteht Konkurrenz um Nährstoffe oder Sauerstoff. Dann haben die Bakterien Vorteile, die sich durch Mutationen an die Bedingungen anpassen oder die anderen Typen zurückdrängen können.
"Ein Stamm produziert eine antibiotisch wirksame Substanz, die Selektionsdruck auf die anderen ausübt und ihm selbst einen Wachstumsvorteil verschafft. Darauf reagieren die anderen Bakterien mit Mutationen, um der Wirkung der Substanz zu entgehen. Ein solcher Stamm kann dann auch resistent gegen andere Antibiotika sein."
Kettenreaktion im Mutationsexperiment
Eine solche Kettenreaktion haben die Würzburger Forscher auch in einem ihrer Mutationsexperimente beobachtet. Einer der weißen Mutantenstämme schien dabei Wachstumsvorteile gegenüber dem orangenen Wildtyp zu haben. Nach einer Weile bildeten sich auf der Agarplatte außerdem Kolonien von hellgelben Bakterien, die sogar noch besser wuchsen als die weißen. Als die Forscher genauer hinsahen, entdeckten sie, dass der weiße Stamm antibiotisch wirksame Stoffe abgab, die den orangen zurückdrängten. Dem hellgelben Stamm konnten diese Stoffe dagegen nichts anhaben, er hatte eine Resistenz entwickelt.
"Sie müssen sich anpassen. Und die Folge davon ist die Entstehung eines robusteren Stammes, der sehr schwer zu bekämpfen ist."
Der hellgelbe Stamm erwies sich als ein solcher Fall. Die Mutation schützte ihn nicht nur vor dem Stoff des weißen Konkurrenten, sondern auch vor dem Antibiotikum Vancomycin, obwohl die Bakterien nie damit in Kontakt gekommen waren. Da Vancomycin eigentlich als letztes Mittel eingesetzt wird, wenn andere Antibiotika nicht mehr wirken, ist eine solche Resistenz medizinisch besonders problematisch. Für Daniel Lopez ein Grund, Biofilme noch gezielter zu bekämpfen.
"In Bakterienkolonien können durch die Konkurrenz spontane Resistenzen gegen Antibiotika entstehen. Das ist etwas, das wir berücksichtigen sollten. Wir sollten unsere antimikrobiellen Strategien entsprechend anpassen, um zu verhindern, dass die Kolonien überhaupt die Stadien erreichen, in denen solche Wechselwirkungen stattfinden."
Das ist besonders in Krankenhäusern wichtig. Da Staphylokokken auch auf der Haut siedeln, können sie beim Einsetzen von Kathedern oder künstlichen Gelenken ins Innere des Körpers gelangen, dort Resistenzen entwickeln und schwer zu behandelnde Infektionen auslösen. Daniel Lopez hofft, dass das in Zukunft verhindert werden kann.