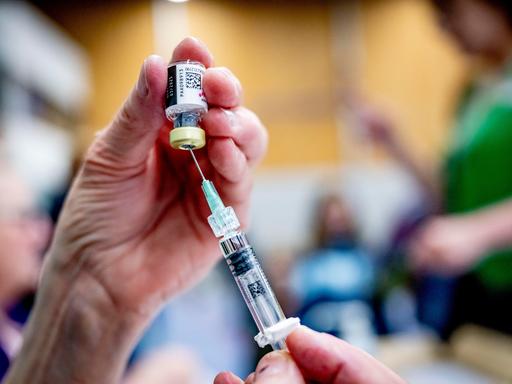
In Deutschland ist Krebs die zweihäufigste Todesursache. Die Entwicklung eines Impfstoffs gegen Krebs ist zwar keine neue Idee, doch den entscheidenden Durchbruch brachte die COVID-19-Pandemie: Sie ermöglichte Unternehmen wie Biontech und Moderna, die mRNA-Technologie zu optimieren und in großem Maßstab zu produzieren. Die während der Pandemie erzielten Gewinne dienen nun als finanzielle Basis für umfangreiche klinische Studien zur Anwendung von mRNA in der Krebsbekämpfung.
Inhalt
- Was ist die mRNA-Technologie und wie funktioniert sie in der Krebsforschung?
- Für welche Krebsarten könnte die mRNA-Impfung eingesetzt werden?
- Wie läuft eine Behandlung mit mRNA-Technologie ab, gibt es Nebenwirkungen?
- Wie ist der aktuelle Stand der Studien, gibt es schon Erfolge mit mRNA-Impfungen?
- Wann könnte die erste mRNA-Krebsimpfung voraussichtlich zugelassen werden?
- Welche Herausforderungen gibt es noch?
Was ist die mRNA-Technologie und wie funktioniert sie in der Krebsforschung?
Was einst als Ansatz zur Behandlung alltäglicher Beschwerden wie Blasen am Fuß gedacht war, hat sich dank der Forschung von Nobelpreisträgerin Katalin Karikó an dem Biomolekül mRNA zu einer vielversprechenden Strategie zur Bekämpfung großer Volkskrankheiten wie Krebs entwickelt.
Das „M“ in mRNA steht für „Messenger“ – ein Botenmolekül, das wichtige Informationen übermittelt. „Und diese Informationen dienen hierzu wie quasi Baupläne, um Proteine herzustellen, die für verschiedene Funktionen im Körper benötigt werden“, erklärt Luisa Manning, Executive Medical Director bei Biontech.
Krebszellen entstehen durch genetische Veränderungen, die ihr unkontrolliertes Wachstum ermöglichen und oft erst spät vom Immunsystem erkannt werden. In der Krebsforschung wird mRNA so „programmiert“, dass sie dem Körper den Bauplan für spezielle Merkmale von Krebszellen - Neoantigene – übermittelt.
Das Immunsystem erkennt daraufhin diese Merkmale als fremd und lernt, die Krebszellen gezielt zu bekämpfen, so Manning . Das Ziel ist es, das Immunsystem so zu trainieren, dass es selbst kleinste Krebsreste erkennt und vernichtet, um Rückfälle zu verhindern. Gelingt dies, kann der Krebs nicht zurückkommen und der Patient gilt als geheilt.
mRNA-Impfung als Therapie - nicht zur Krebsprävention
Im Gegensatz zu einer Präventivimpfung wie der HPV-Impfung gegen Gebärmutterhalskrebs kommt die mRNA-Impfung als Therapie zum Einsatz, vor allem dann, wenn nur noch möglichst wenig Tumor im Körper ist, erläutert Niels Halama vom Deutschen Krebsforschungszentrum. Der große Vorteil: „Während bei der Corona-Impfung jeder die gleiche Impfung bekommen hat, ist es mit mRNA möglich, das Ganze jetzt so zu personalisieren, dass jeder einzelne Patient seinen ganz speziellen Impfstoff bekommt.“
Da der Körper durch die mRNA das benötigte Protein selbst herstellt, entfällt ein aufwendiger Produktionsschritt im Labor. Die Entwicklung könnte dadurch schneller und kostengünstiger erfolgen. Trotzdem werden personalisierte mRNA-Therapien voraussichtlich sehr teuer werden. Möglich sind auch vordefinierte Impfstoffe mit mRNA-Molekülen, die auf Neoantigene abzielen, die bei vielen Patienten mit einer bestimmten Krebsart vorkommen. Dieser Impfstoff könnte vorproduziert und somit sofort verfügbar sein („off-the-shelf“).
Für welche Krebsarten könnte die mRNA-Impfung eingesetzt werden?
Die Grundvoraussetzung für den Einsatz der mRNA-Krebstherapie ist, dass ausreichend Tumorgewebe für die Analyse verfügbar ist. Dann könnte die Methode bei sehr vielen, wenn nicht sogar allen Krebsarten zum Einsatz kommen, sagt Niels Halama vom Deutschen Krebsforschungszentrum.
Er sieht in der mRNA-Therapie einen „Fortschritt“ in der Onkologie und bestätigt: Selbst Erkrankungen, die bisher als unbehandelbar galten, könnten durch diese ersten Schritte in der Immuntherapie nun doch behandelbar werden. Derzeit konzentriert sich die Forschung vor allem auf schwarzen Hautkrebs (Melanom), Darmkrebs und den besonders aggressiven Bauchspeicheldrüsenkrebs.
Wie läuft eine Behandlung mit mRNA-Technologie ab, gibt es Nebenwirkungen?
Die mRNA-Krebsimpfstoffe basieren auf derselben Grundtechnologie wie die COVID-19- mRNA-Impfstoffe, sind aber auf die Tumore der Patienten zugeschnitten: Zunächst entnehmen Ärzte Tumorgewebe, das im Labor analysiert wird, um die Unterschiede zu gesunden Zellen zu identifizieren. Auf dieser Basis wird ein passender mRNA-Impfstoff entwickelt, der „Fahndungsfotos“ der Tumormerkmale enthält.
Eingepackt in winzige Fettkügelchen (Lipoplexe) gelangt er gezielt ins Immunsystem. Die Fetthülle schützt die empfindliche mRNA vor schnellem Abbau im Körper. Nachdem sie ihre Aufgabe erfüllt hat, wird die mRNA von Enzymen wieder zerlegt, verbleibt somit nicht im Körper und verändert auch kein Erbgut. „Unsere Technologie ist so entwickelt, dass dann die mRNA genau an den Ort transportiert werden kann, wo wir sie brauchen, wie zum Beispiel unsere Lymphorgane und die Milz“, beschreibt Luisa Manning von Biontech diesen Transportmechanismus.
Die Behandlung beinhaltet mehrere Impfdosen und wird häufig mit Antikörperpräparaten, Chemotherapie, Checkpoint-Inhibitoren oder anderen Immuntherapien kombiniert. Checkpoint-Inhibitoren sind Medikamente, die bestimmte Bremsen im Immunsystem („Checkpoints“) lösen. Dadurch können Immunzellen wieder Tumorzellen angreifen. Allerdings spricht nur etwa die Hälfte der Patienten darauf an, weil bei vielen eine Immunresistenz vorliegt: Ihr Immunsystem reagiert trotz gelöster Bremse nicht. mRNA-Impfstoffe können hier unterstützen, indem sie dem Immunsystem gezielt zeigen, welche Krebszellen es bekämpfen soll.
Die Nebenwirkungen sind denen der COVID-19-Impfungen ähnlich: grippale Beschwerden wie Fieber, Schmerzen an der Einstichstelle.
Wie ist der aktuelle Stand der Studien, gibt es schon Erfolge mit mRNA-Impfungen?
Weltweit laufen zahlreiche Studien, Deutschland ist dabei Vorreiter. Erste Ergebnisse sind vielversprechend. Besonders beim Bauchspeicheldrüsenkrebs, einer bisher nur schwer therapierbaren Krebsart, konnten in einer kleinen Studie beachtliche Erfolge erzielt werden: Patienten, die auf eine Impfung ansprachen, hatten keinen Rückfall. Das wäre ein möglicher Meilenstein bei dieser oft tödlichen Erkrankung.
Allerdings zeigten die Impfungen nicht bei allen Betroffenen Wirkung. Hier sind größere Studien nötig. Auch bei schwarzem Hautkrebs lassen die bisherigen Ergebnisse auf eine wirksame Therapie hoffen. Dennoch bremsen Experten: mRNA ist keine Wunderwaffe.
Wann könnte die erste mRNA-Krebsimpfung voraussichtlich zugelassen werden?
Die Zulassung hängt vom erfolgreichen Abschluss der klinischen Studien ab, die sich in der Regel über Jahre ziehen. Experten halten eine Zulassung frühestens 2026 bis 2027 für realistisch - wohl zuerst für schwarzen Hautkrebs. Für andere Krebsarten befinden sich die Studien noch in einem früheren Stadium.
Welche Herausforderungen gibt es noch?
Die Wirksamkeit und die Sicherheit müssen zunächst in großen Phase-3-Studien belegt werden. Zudem ist noch unklar, wie dauerhaft die Immunantwort durch die mRNA-Therapie ist, da Langzeitdaten fehlen.
Christoffer Gebhardt, stellvertretender Direktor der Klinik für Dermatologie an der Universität Hamburg-Eppendorf und Leiter einer Studie von Moderna, weist zudem auf die Kosten hin. Die Herstellung ist teuer und komplex – bei individualisierten Impfstoffen könnten die Kosten pro Patient bei über 100.000 Euro pro Jahr liegen. Das ist ein Betrag, der voraussichtlich zu intensiven Diskussionen im Gesundheitssystem führen wird.
og