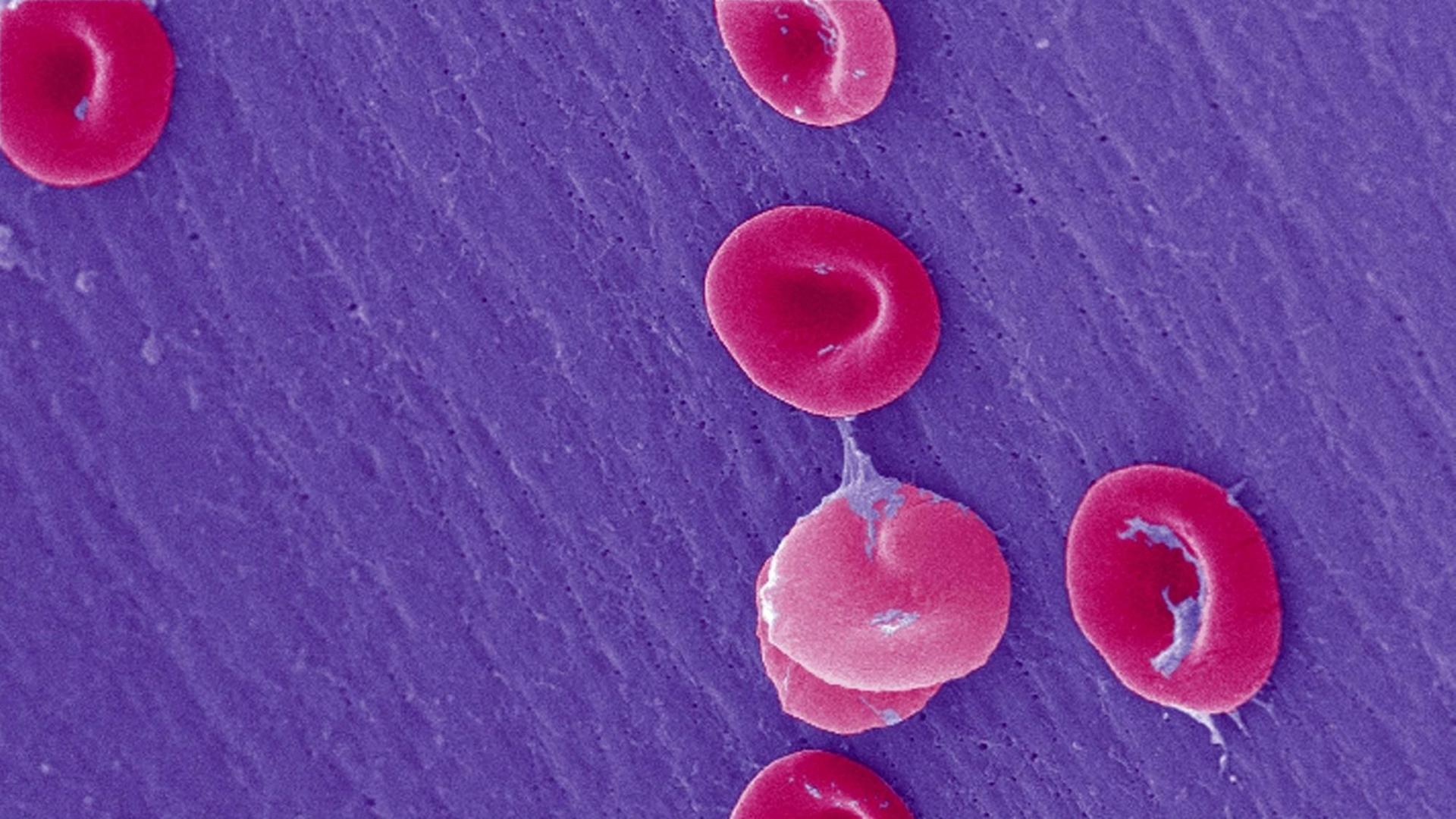
Die Sichelzellkrankheit ist eine Erbkrankheit, die vor allem im Malaria-Gürtel verbreitet ist. Denn die Gen-Mutation bietet einen Überlebensvorteil: Sie schützt vor Malaria. Wer die Mutation nicht nur von Vater oder Mutter erbt, sondern von beiden, bei dem bricht die Krankheit aus. Die sichelförmigen Blutkörperchen bleiben in den Blutgefäßen stecken, die Organe bekommen zu wenig Sauerstoff. Mehrere Male im Jahr macht sich die Krankheit mit starken Schmerzen bemerkbar.
"Eine Krise, so nennt man den Sichelzell-Schmerz, eine Krise trifft normalerweise die Knochen oder Gelenke. Jeder Körperteil kann betroffen sein, aber ich hatte es immer in meinen Extremitäten, in meinen Armen und Beinen. Das fühlt sich an, als würde jemand meinen Arm ununterbrochen mit einem Presslufthammer bearbeiten. Es fängt milde an und wird dann schlimmer und schlimmer. Stellen Sie sich vor, jemand hämmert auf Ihren Arm, immer weiter. So schlimm sind die Schmerzen."
Yetunde Olagbaju wurde in Nigeria mit der Erbkrankheit geboren. Ihre Eltern hatten die Möglichkeit in die USA einzuwandern, wo sie sich eine bessere medizinische Versorgung für ihre Tochter versprachen. Doch selbst hier liegt die Lebenserwartung für die 90.000 Sichelzell-Patienten bei nur etwa 45 Jahren. Thrombosen, Schlaganfälle, Organversagen sind häufige Todesursachen. Während einer Krise sind die Patienten auf starke Schmerzmittel angewiesen, die abhängig machen. Yetunde Olagbaju:
"Ich habe immer versucht, so ruhig wie möglich zu liegen, mit Heizdecken oder einer Wärmflasche und Schmerzmitteln. Und wenn die Pillen zu Hause nicht stark genug sind, dann kommen wir ins Krankenhaus und bekommen eine Infusion mit Schmerzmitteln und auch Sauerstoff, was auch hilft, weil der Körper ja Sauerstoffmangel hat, weshalb die Schmerzen angefangen haben."
"Eine Krise, so nennt man den Sichelzell-Schmerz, eine Krise trifft normalerweise die Knochen oder Gelenke. Jeder Körperteil kann betroffen sein, aber ich hatte es immer in meinen Extremitäten, in meinen Armen und Beinen. Das fühlt sich an, als würde jemand meinen Arm ununterbrochen mit einem Presslufthammer bearbeiten. Es fängt milde an und wird dann schlimmer und schlimmer. Stellen Sie sich vor, jemand hämmert auf Ihren Arm, immer weiter. So schlimm sind die Schmerzen."
Yetunde Olagbaju wurde in Nigeria mit der Erbkrankheit geboren. Ihre Eltern hatten die Möglichkeit in die USA einzuwandern, wo sie sich eine bessere medizinische Versorgung für ihre Tochter versprachen. Doch selbst hier liegt die Lebenserwartung für die 90.000 Sichelzell-Patienten bei nur etwa 45 Jahren. Thrombosen, Schlaganfälle, Organversagen sind häufige Todesursachen. Während einer Krise sind die Patienten auf starke Schmerzmittel angewiesen, die abhängig machen. Yetunde Olagbaju:
"Ich habe immer versucht, so ruhig wie möglich zu liegen, mit Heizdecken oder einer Wärmflasche und Schmerzmitteln. Und wenn die Pillen zu Hause nicht stark genug sind, dann kommen wir ins Krankenhaus und bekommen eine Infusion mit Schmerzmitteln und auch Sauerstoff, was auch hilft, weil der Körper ja Sauerstoffmangel hat, weshalb die Schmerzen angefangen haben."
Hoffnung auf Heilung durch CRISPR /Cas
Dieses Leid wollen Wissenschaftler nun ein für alle Mal beenden: mit CRISPR /Cas, einer hochpräzisen Schere, die bislang für Gentherapien am Menschen noch nicht zum Einsatz kam.
"Die Genetik hinter der Sichelzellkrankheit ist seit 1949 bekannt. Also seit über 70 Jahren wissen wir genau, wie Sichelzellkrankheit auf genetischer Ebene funktioniert. Es ist eine Mutation an einem einzigen Punkt im Genom eines Menschen. Es gibt eine riesige Menge Daten, die zeigen, dass diese Mutation die alleinige Ursache ist. Das heißt theoretisch, dass man ganz einfach nur diese Base austauschen muss, und schon ist die Krankheit geheilt."
Seit Jahrzehnten ringt die Medizin um Gentherapien. Die Liste der Rückschläge ist lang, aber jetzt wurden für seltene Muskelleiden oder Augenkrankheiten wie die Makula-Degeneration erste Gentherapien zugelassen - nach aufwändiger, langer, teurer Forschung. Mit Hilfe der hochpräzisen CRISPR-Schere könnte das Feld explodieren. Wie am Fließband wollen Mediziner damit eine Erbkrankheit nach der anderen heilen. Jacob Corn vom Innovative Genomics Institute der Universitäten Berkeley und San Francisco ist euphorisch und Mark Walters, der am Kinderkrankenhaus der Universität von Kalifornien in Oakland Sichelzell-Patienten versorgt, geht es nicht anders:
"Ja, das ist der Heilige Gral. Davon haben wir im Studium geträumt, dass man eine Mutation erkennt, sie direkt korrigiert und somit die Krankheit kuriert."
"Die Genetik hinter der Sichelzellkrankheit ist seit 1949 bekannt. Also seit über 70 Jahren wissen wir genau, wie Sichelzellkrankheit auf genetischer Ebene funktioniert. Es ist eine Mutation an einem einzigen Punkt im Genom eines Menschen. Es gibt eine riesige Menge Daten, die zeigen, dass diese Mutation die alleinige Ursache ist. Das heißt theoretisch, dass man ganz einfach nur diese Base austauschen muss, und schon ist die Krankheit geheilt."
Seit Jahrzehnten ringt die Medizin um Gentherapien. Die Liste der Rückschläge ist lang, aber jetzt wurden für seltene Muskelleiden oder Augenkrankheiten wie die Makula-Degeneration erste Gentherapien zugelassen - nach aufwändiger, langer, teurer Forschung. Mit Hilfe der hochpräzisen CRISPR-Schere könnte das Feld explodieren. Wie am Fließband wollen Mediziner damit eine Erbkrankheit nach der anderen heilen. Jacob Corn vom Innovative Genomics Institute der Universitäten Berkeley und San Francisco ist euphorisch und Mark Walters, der am Kinderkrankenhaus der Universität von Kalifornien in Oakland Sichelzell-Patienten versorgt, geht es nicht anders:
"Ja, das ist der Heilige Gral. Davon haben wir im Studium geträumt, dass man eine Mutation erkennt, sie direkt korrigiert und somit die Krankheit kuriert."
"Das ist der Heilige Gral"
Mark Walters und Jacob Corn gehören zu einer von mehreren Forschergruppen, die 2019 oder 2020 mit klinischen Studien für experimentelle CRISPR-Behandlungen beginnen wollen. Die Sichelzellkrankheit haben sich alle diese Forschergruppen als erste Erbkrankheit vorgenommen. Denn ihre Ursache ist eine einzelne Mutation und nicht eine komplexe Kombination von Genen. Und sie ist so gut erforscht, dass die Forscher genau wissen, wo in den Stammzellen sie ansetzen müssen - theoretisch. Praktisch ist die Therapie Neuland.
Die Stammzellen sitzen im Knochenmark fest, und müssen erst einmal aus dem Körper eines Patienten gewonnen werden, um sie später im Labor zu korrigieren, erzählt Mark Walters.
"Wir leiten das Blut aus dem Körper heraus, sammeln die Stammzellen mit einem Gerät und leiten die Bestandteile, die wir nicht brauchen, zurück in den Blutkreislauf. Das ist der erste Schritt.
Dann geht der Patient nach Hause, während im Labor die Genmanipulation passiert. Die Stammzellen werden isoliert, gereinigt, und dann kommen die Reagenzien hinzu, das CRISPR-Cas9 und die korrigierte Kopie der DNA-Mutation. Die Zellen werden einem elektrischen Puls ausgesetzt, damit die Reagenzien in den Zellkern eindringen, wo sie die Korrektur vornehmen. Der ganze Prozess geht ziemlich schnell und 48 Stunden später werden die Zellen schon für die Transplantation eingefroren. In der letzten Phase kommt dann der Patient zurück. Wenn wir sichergestellt haben, dass die Zellen lebensfähig sind, die Korrektur wie erwartet funktioniert hat und es keine Verunreinigungen mit Mikroorganismen gibt, dann bekommt der Patient eine hohe Dosis Chemotherapie, um die Sichelzellen produzierenden Stammzellen in seinem Körper zu zerstören. Wenn das abgeschlossen ist, tauen wir einfach die korrigierten Stammzellen auf und bringen sie zurück in den Blutkreislauf, wie bei einer Transfusion."
Vier bis sechs Wochen soll es dauern, bis sich die Blut-Stammzellen im Knochenmark angesiedelt haben. Die neuen Blutkörperchen, die sie produzieren, verformen sich nicht mehr zu harten, klebrigen Sicheln. Der Patient ist geheilt. Allerdings muss er sein Immunsystem neu aufbauen, denn das wurde durch die Chemotherapie zerstört.
"Wir leiten das Blut aus dem Körper heraus, sammeln die Stammzellen mit einem Gerät und leiten die Bestandteile, die wir nicht brauchen, zurück in den Blutkreislauf. Das ist der erste Schritt.
Dann geht der Patient nach Hause, während im Labor die Genmanipulation passiert. Die Stammzellen werden isoliert, gereinigt, und dann kommen die Reagenzien hinzu, das CRISPR-Cas9 und die korrigierte Kopie der DNA-Mutation. Die Zellen werden einem elektrischen Puls ausgesetzt, damit die Reagenzien in den Zellkern eindringen, wo sie die Korrektur vornehmen. Der ganze Prozess geht ziemlich schnell und 48 Stunden später werden die Zellen schon für die Transplantation eingefroren. In der letzten Phase kommt dann der Patient zurück. Wenn wir sichergestellt haben, dass die Zellen lebensfähig sind, die Korrektur wie erwartet funktioniert hat und es keine Verunreinigungen mit Mikroorganismen gibt, dann bekommt der Patient eine hohe Dosis Chemotherapie, um die Sichelzellen produzierenden Stammzellen in seinem Körper zu zerstören. Wenn das abgeschlossen ist, tauen wir einfach die korrigierten Stammzellen auf und bringen sie zurück in den Blutkreislauf, wie bei einer Transfusion."
Vier bis sechs Wochen soll es dauern, bis sich die Blut-Stammzellen im Knochenmark angesiedelt haben. Die neuen Blutkörperchen, die sie produzieren, verformen sich nicht mehr zu harten, klebrigen Sicheln. Der Patient ist geheilt. Allerdings muss er sein Immunsystem neu aufbauen, denn das wurde durch die Chemotherapie zerstört.
Risiken und Nebenwirkungen – eher Nebensache?
Die Nebenwirkungen der gesamten Prozedur sind heftig. Darauf angesprochen antworten die Forscher von Innovative Genomics eher kurz angebunden. Andere, wie das börsennotierte Startup CRISPR Therapeutics, geben erst gar kein Interview. Schlechte Nachrichten über Risiken von CRISPR haben schon öfter den Aktienkurs der Firma fallen lassen. Das Unternehmen schien anderen Forschergruppen weit voraus, beantragte als erstes eine klinische Studie für eine CRISPR-basierte Therapie für Sichelzellkrankheit. Mitte 2018 legte die Aufsichtsbehörde FDA den Antrag aus unbekannten Gründen auf Eis. Inzwischen aber läuft die Studie an. Jetzt stehen CRISPR Therapeutics und die anderen Entwickler-Gruppen vor dem Problem, dass sie Patienten rekrutieren müssen. Nicht nur wegen der Risiken und Nebenwirkungen dürfte das eine Herausforderung sein..
"Wir haben hier eine Gruppe von Menschen, die vom System missbraucht wurden. Die werden dem System nicht mehr vertrauen. Das würde keinen Sinn machen."
Harriet Washington ist Autorin des Buchs Medical Apartheid. Darin beschreibt sie, wie Afroamerikaner von der Sklaverei bis heute von Medizinern misshandelt wurden. Während dieser 300 Jahre wurden sie immer wieder für Studien missbraucht, von deren Ergebnissen sie nicht profitierten.
"Wir haben hier eine Gruppe von Menschen, die vom System missbraucht wurden. Die werden dem System nicht mehr vertrauen. Das würde keinen Sinn machen."
Harriet Washington ist Autorin des Buchs Medical Apartheid. Darin beschreibt sie, wie Afroamerikaner von der Sklaverei bis heute von Medizinern misshandelt wurden. Während dieser 300 Jahre wurden sie immer wieder für Studien missbraucht, von deren Ergebnissen sie nicht profitierten.
Afroamerikaner: Patient oder Versuchskanninchen?
"Niemand verliert mehr Arme und Beine, nur um Medizinstudenten zu zeigen, wie man eine Amputation durchführt. Die schlimmsten Arten von Missbrauch sind vorbei. Leider haben wir neue gefunden, um sie zu ersetzen. Unsere Medizinforschung erlaubt immer noch unethische Studien, die vor allem für Minderheiten und Randgruppen ein größeres Risiko und geringeren Nutzen bedeuten als für die Gesamtbevölkerung. Missbräuchliche, unethische und ehrlich gesagt unwissenschaftliche Studien werden immer noch genehmigt."
Wenn Menschen dem Gesundheitssystem skeptisch gegenüber stehen, dann nicht nur wegen der Vergangenheit, sondern auch wegen der Gegenwart, sagt Harriet Washington. Wer sind die Profiteure diesmal? Probanden haben jedes Recht misstrauisch zu sein, ob ihr Wohl im Mittelpunkt steht oder Aktienkurse von CRISPR-Startups oder Forscherkarrieren. Mark Walters und Jacob Corn, die die CRISPR-Studie in Kalifornien durchführen wollen, sind sich dessen bewusst.
Mark Walters: "Ich respektiere, dass es wichtig ist, für die Sicherheit der Patienten zu sorgen. Und da sind wir bei der Sichelzell-Krankheit, die in diesem Land vor allem Afroamerikaner betrifft, besonders vorsichtig. Es gibt ein gewisses Stigma in dieser ethnischen Gruppe gegenüber medizinischer Forschung. Skepsis. Das respektiere ich und mir ist klar, dass wir die Forschung nur partnerschaftlich mit Patienten und ihren Familien vorantreiben können."
Jacob Corn: "Ich denke, wir eröffnen Menschen eine Option und wollen sehr offen damit umgehen. Wir würden nie versuchen jemandem nahezulegen, diese Behandlung zu machen oder nicht."
Dass Walters und Corn hier von Patienten und von einer Behandlung sprechen, irritiert Harriet Washington allerdings.
"Das nennt sich Behandlungs-Illusion und ist in der Medizinforschung in den USA weit verbreitet. Die Begeisterung für eine potentiell wirksame Behandlung oder sogar eine Heilung der Sichelzellkrankheit ist wunderbar, aber es ist wichtig, diese Begeisterung nicht zu einer Behandlungs-Illusion werden zu lassen, sodass die Teilnehmer denken, sie erhalten eine Behandlung, wo sie in Wirklichkeit Forschungs-Gegenstand sind."
Wenn Menschen dem Gesundheitssystem skeptisch gegenüber stehen, dann nicht nur wegen der Vergangenheit, sondern auch wegen der Gegenwart, sagt Harriet Washington. Wer sind die Profiteure diesmal? Probanden haben jedes Recht misstrauisch zu sein, ob ihr Wohl im Mittelpunkt steht oder Aktienkurse von CRISPR-Startups oder Forscherkarrieren. Mark Walters und Jacob Corn, die die CRISPR-Studie in Kalifornien durchführen wollen, sind sich dessen bewusst.
Mark Walters: "Ich respektiere, dass es wichtig ist, für die Sicherheit der Patienten zu sorgen. Und da sind wir bei der Sichelzell-Krankheit, die in diesem Land vor allem Afroamerikaner betrifft, besonders vorsichtig. Es gibt ein gewisses Stigma in dieser ethnischen Gruppe gegenüber medizinischer Forschung. Skepsis. Das respektiere ich und mir ist klar, dass wir die Forschung nur partnerschaftlich mit Patienten und ihren Familien vorantreiben können."
Jacob Corn: "Ich denke, wir eröffnen Menschen eine Option und wollen sehr offen damit umgehen. Wir würden nie versuchen jemandem nahezulegen, diese Behandlung zu machen oder nicht."
Dass Walters und Corn hier von Patienten und von einer Behandlung sprechen, irritiert Harriet Washington allerdings.
"Das nennt sich Behandlungs-Illusion und ist in der Medizinforschung in den USA weit verbreitet. Die Begeisterung für eine potentiell wirksame Behandlung oder sogar eine Heilung der Sichelzellkrankheit ist wunderbar, aber es ist wichtig, diese Begeisterung nicht zu einer Behandlungs-Illusion werden zu lassen, sodass die Teilnehmer denken, sie erhalten eine Behandlung, wo sie in Wirklichkeit Forschungs-Gegenstand sind."
Alternative: Knochenmarkstransplantation
Studienteilnehmer genießen nicht denselben Schutz wie Patienten, warnt sie. Anders als bei einer Behandlung seien Risiken und Nebenwirkungen noch unbekannt. Hinzu kommt: Es gibt schon eine Heilmethode für die Sichelzellkrankheit. Sie heißt Knochenmarktransplantation.
"Ich habe von Knochenmarktransplantationen durch den Freund meines besten Freundes gehört. Dessen Bruder hatte Sichelzellen. Er hat das durchgemacht an einem Krankenhaus, wo sie auch Minderjährige transplantieren. Und leider hat er es nicht überlebt. Er hatte schreckliche Komplikationen durch die Knochenmarktransplantation. Seine Lungen funktionierten nicht mehr und er brauchte eine Lungentransplantation, aber er hat es nicht geschafft. Also, er ist an der Knochenmarktransplantation gestorben. Also dachte ich mir, das will ich nicht machen. Ich kenne jemanden, der daran gestorben ist."
Aber kurz nachdem Yetunde Olagbaju ihren College-Abschluss hatte, verschlechterte sich ihr Zustand. Stress kann zu den Auslösern gehören und während ihres ersten Vollzeitjobs verbrachte sie Monate im Krankenhaus. Die Krisen der Sichelzellkrankheit wurden schlimmer: eine Lungenentzündung nach der anderen. Die Krankheit wurde lebensbedrohlich. Lebensbedrohlicher als eine Knochenmarktransplantation.
"Wir hatten ein Familientreffen und haben beschlossen, es durchzuziehen."
"Ich habe von Knochenmarktransplantationen durch den Freund meines besten Freundes gehört. Dessen Bruder hatte Sichelzellen. Er hat das durchgemacht an einem Krankenhaus, wo sie auch Minderjährige transplantieren. Und leider hat er es nicht überlebt. Er hatte schreckliche Komplikationen durch die Knochenmarktransplantation. Seine Lungen funktionierten nicht mehr und er brauchte eine Lungentransplantation, aber er hat es nicht geschafft. Also, er ist an der Knochenmarktransplantation gestorben. Also dachte ich mir, das will ich nicht machen. Ich kenne jemanden, der daran gestorben ist."
Aber kurz nachdem Yetunde Olagbaju ihren College-Abschluss hatte, verschlechterte sich ihr Zustand. Stress kann zu den Auslösern gehören und während ihres ersten Vollzeitjobs verbrachte sie Monate im Krankenhaus. Die Krisen der Sichelzellkrankheit wurden schlimmer: eine Lungenentzündung nach der anderen. Die Krankheit wurde lebensbedrohlich. Lebensbedrohlicher als eine Knochenmarktransplantation.
"Wir hatten ein Familientreffen und haben beschlossen, es durchzuziehen."
Das Problem des passenden Spenders
Ihr Bruder spendete das Knochenmark. Er hat nur eine Kopie der Sichelzell-Mutation von den Eltern geerbt, nicht zwei wie seine Schwester. Das war vor acht Jahren. Seitdem ist Yetunde Olagbaju gesund. Nicht jeder will das Risiko eingehen und nicht immer findet sich ein passender Spender. Zumindest dieses Problem würde die CRISPR-Therapie lösen.
Jacob Corn: "Was wir machen wollen, ist auch eine Knochenmarktransplantation, aber die Leute sind ihre eigenen Spender. Wir ermöglichen es, das eigene Knochenmark zu nehmen, zu editieren und dann zurückzugeben. Man muss also nicht nach einem Spender suchen, sondern sie sind selbst der Spender."
Andererseits ist die Suche in den letzten Jahren einfacher geworden. Robert Brodsky, der auch Yetunde Olagbaju transplantiert hat, hat am Johns Hopkins Hospital in Baltimore eine Methode entwickelt, bei der der Spender nicht mehr ein hundertprozentiger Treffer sein muss, sondern nur ein halber Treffer, wie er es formuliert.
"Wir können einen Bruder nehmen, eine Schwester, ein Elternteil, ein Kind, eine Tante, eine Nichte. Selbst wenn sie eine Kopie der Sichelzell-Mutation haben, können sie Spender sein. Die meisten Patienten haben jetzt die Möglichkeit einer Knochenmarktransplantation."
Jacob Corn: "Was wir machen wollen, ist auch eine Knochenmarktransplantation, aber die Leute sind ihre eigenen Spender. Wir ermöglichen es, das eigene Knochenmark zu nehmen, zu editieren und dann zurückzugeben. Man muss also nicht nach einem Spender suchen, sondern sie sind selbst der Spender."
Andererseits ist die Suche in den letzten Jahren einfacher geworden. Robert Brodsky, der auch Yetunde Olagbaju transplantiert hat, hat am Johns Hopkins Hospital in Baltimore eine Methode entwickelt, bei der der Spender nicht mehr ein hundertprozentiger Treffer sein muss, sondern nur ein halber Treffer, wie er es formuliert.
"Wir können einen Bruder nehmen, eine Schwester, ein Elternteil, ein Kind, eine Tante, eine Nichte. Selbst wenn sie eine Kopie der Sichelzell-Mutation haben, können sie Spender sein. Die meisten Patienten haben jetzt die Möglichkeit einer Knochenmarktransplantation."
Heilung ist möglich. Folgeerkrankungen auch.
90 bis 95 Prozent würden einen Spender finden, sagt Brodsky. Bei herkömmlichen Knochenmark-Transplantationen gibt es für weniger als 20 Prozent der Patienten Spender. Das ist eine Zahl, die die CRISPR-Forscher ins Feld führen und so die potenzielle Zielgruppe ihrer Technik vergrößern. Doch sie müssen sich an der Arbeit von Robert Brodsky und der Knochenmarktransplantation ohne Genmodifikation messen lassen. Mit Nutzen – und Nebenwirkung. Denn die könnte auch bei CRISPR alles andere als harmlos sein, gibt Mark Walters zu:
"Was uns am meisten Sorgen macht ist, dass Blutstammzellen ein Leben lang Blutkörperchen produzieren. Und wir wissen, dass sie wohl auch die Quelle von Leukämie oder Blutkrebs sind. Wenn wir jetzt deren Genom manipulieren, müssen wir sehr vorsichtig sein, dass wir da nicht ein Problem beseitigen, die Sichelzellenanämie, aber ein schlimmeres Problem verursachen: Blutkrebs."
Eine andere Sorge von Mark Walters sind im Sommer 2018 erschienene Studien, die nahelegen, dass ausgerechnet die Blutstammzellen, die sich besonders leicht mit der CRISPR-Technik manipulieren lassen, eher Krebs entwickeln. Und schließlich ist unklar, wie genau die Genschere CRISPR tatsächlich schneidet. Möglicherweise verursacht sie Schäden am Erbgut an Stellen weit entfernt von der eigentlichen Schnittstelle.
"Ich werde immer wieder gefragt: Doktor, was ist die Erfolgsquote? Wie groß ist Ihre Erfahrung? Wie oft haben Sie das schon gemacht? Stellen Sie sich vor zu antworten: Ich weiß nicht, was die Erfolgsquote ist und Sie sind der erste Patient, den ich behandeln werde. Das ist beängstigend. Das wäre für mich beängstigend. Deshalb sage ich: Es beruht auf dem Mut von ein paar Individuen, die es satt haben, Sichelzellanämie zu haben und die sich der Weiterentwicklung dieses Gebiets verschrieben haben und dem Team vertrauen, das die Prozedur durchführt."
Um dieses Vertrauen aufzubauen, treffen sich die Forscher mit Patientengruppen. Sie gehen informiert in diese Treffen. Die rassistische Behandlung von Afroamerikanern durch die Medizin in vergangenen Jahrzehnten und Jahrhunderten ist ihnen bewusst. Mark Walters glaubt aber, dass gerade CRISPR das Blatt wenden könnte:
"Der Eindruck ist, dass weil diese Krankheit in unserem Land vor allem Afroamerikaner betrifft, sie nicht die Aufmerksamkeit bekommt, die sie verdient, dass die Forschung nicht so intensiv ist, wie sie sein sollte, und dass es unserer Gesellschaft nicht genauso wichtig war, eine Heilung zu finden, wie es bei Krebs der Fall ist. Das muss sich ändern, und ich glaube, dass wir das jetzt endlich angehen mit diesen vielfältigen Behandlungsmethoden, die jetzt entwickelt werden."
Eine andere Sorge von Mark Walters sind im Sommer 2018 erschienene Studien, die nahelegen, dass ausgerechnet die Blutstammzellen, die sich besonders leicht mit der CRISPR-Technik manipulieren lassen, eher Krebs entwickeln. Und schließlich ist unklar, wie genau die Genschere CRISPR tatsächlich schneidet. Möglicherweise verursacht sie Schäden am Erbgut an Stellen weit entfernt von der eigentlichen Schnittstelle.
"Ich werde immer wieder gefragt: Doktor, was ist die Erfolgsquote? Wie groß ist Ihre Erfahrung? Wie oft haben Sie das schon gemacht? Stellen Sie sich vor zu antworten: Ich weiß nicht, was die Erfolgsquote ist und Sie sind der erste Patient, den ich behandeln werde. Das ist beängstigend. Das wäre für mich beängstigend. Deshalb sage ich: Es beruht auf dem Mut von ein paar Individuen, die es satt haben, Sichelzellanämie zu haben und die sich der Weiterentwicklung dieses Gebiets verschrieben haben und dem Team vertrauen, das die Prozedur durchführt."
Um dieses Vertrauen aufzubauen, treffen sich die Forscher mit Patientengruppen. Sie gehen informiert in diese Treffen. Die rassistische Behandlung von Afroamerikanern durch die Medizin in vergangenen Jahrzehnten und Jahrhunderten ist ihnen bewusst. Mark Walters glaubt aber, dass gerade CRISPR das Blatt wenden könnte:
"Der Eindruck ist, dass weil diese Krankheit in unserem Land vor allem Afroamerikaner betrifft, sie nicht die Aufmerksamkeit bekommt, die sie verdient, dass die Forschung nicht so intensiv ist, wie sie sein sollte, und dass es unserer Gesellschaft nicht genauso wichtig war, eine Heilung zu finden, wie es bei Krebs der Fall ist. Das muss sich ändern, und ich glaube, dass wir das jetzt endlich angehen mit diesen vielfältigen Behandlungsmethoden, die jetzt entwickelt werden."
Aktivisten für Gleichberechtigung und Pioniere der Medizin
Die gute Absicht, etwas für eine lange vernachlässigte Krankheit zu tun, von der vor allem eine vergleichsweise arme Minderheit im Land betroffen ist, erkennen viele Patienten an. Sie bilden den Gegenpol zu den Skeptikern und lassen sich auch von der ekstatischen Stimmung anstecken, die die rasant voranschreitende CRISPR-Forschung erzeugt. Im Fall der Sichelzellkrankheit ist Michael Friend einer der Vorreiter. Er wurde zum Fürsprecher der Betroffenen, als seine damalige Frau eine Sichelzell-Krise hatte.
Michael Friend und seine Frau fangen damals an zu recherchieren und stoßen schnell auf CRISPR und die damit verbundenen Hoffnungen. Bald danach verbünden sie sich mit einem weiteren Betroffenen: Shakir Cannon. Zusammen gründen sie die Minority Coalition for Precision Medicine, die Minderheiten mit den Möglichkeiten der neuen Gentherapien vertraut machen soll. Über Jahre arbeiten Friend und Cannon intensiv zusammen, telefonieren jeden Tag, um neue Aktivitäten zu planen. Sie werden sogar mehrmals ins Weiße Haus eingeladen, unter anderem zur Vorstellung der Initiative für Präzisionsmedizin von Barack Obama. Ihre Initiative nimmt richtig Fahrt auf - bis zu diesem Tag im Dezember 2017.
"Es war mitten in der Woche, ein Mittwoch, als ich mit Shakir sprach und er sagte, dass er erkältet sei, sich nicht gut fühle. Ich sagte, Mann, wir haben so hart gearbeitet, jahrelang, nimm dir über das Wochenende frei. Lass uns Montag weitermachen. Donnerstag, Freitag gingen vorüber und Samstag bekam ich einen Anruf. Es war seine Handynummer. Seine Frau war dran und sagte, Shakir sei auf der Intensivstation. Ich war schockiert und bat sie, das noch einmal zu sagen. Sie sagte, er sei auf der Intensivstation, es sehe nicht gut aus und er würde es wahrscheinlich nicht überstehen. Ich konnte es nicht glauben. Als ich es nach Albany im Bundesstaat New York geschafft hatte, innerhalb von 24 Stunden, starb er. Das war einer der schwersten Momente meines Lebens und es ist immer noch schwer, so ziemlich jeden Tag."
Michael Friend und seine Frau fangen damals an zu recherchieren und stoßen schnell auf CRISPR und die damit verbundenen Hoffnungen. Bald danach verbünden sie sich mit einem weiteren Betroffenen: Shakir Cannon. Zusammen gründen sie die Minority Coalition for Precision Medicine, die Minderheiten mit den Möglichkeiten der neuen Gentherapien vertraut machen soll. Über Jahre arbeiten Friend und Cannon intensiv zusammen, telefonieren jeden Tag, um neue Aktivitäten zu planen. Sie werden sogar mehrmals ins Weiße Haus eingeladen, unter anderem zur Vorstellung der Initiative für Präzisionsmedizin von Barack Obama. Ihre Initiative nimmt richtig Fahrt auf - bis zu diesem Tag im Dezember 2017.
"Es war mitten in der Woche, ein Mittwoch, als ich mit Shakir sprach und er sagte, dass er erkältet sei, sich nicht gut fühle. Ich sagte, Mann, wir haben so hart gearbeitet, jahrelang, nimm dir über das Wochenende frei. Lass uns Montag weitermachen. Donnerstag, Freitag gingen vorüber und Samstag bekam ich einen Anruf. Es war seine Handynummer. Seine Frau war dran und sagte, Shakir sei auf der Intensivstation. Ich war schockiert und bat sie, das noch einmal zu sagen. Sie sagte, er sei auf der Intensivstation, es sehe nicht gut aus und er würde es wahrscheinlich nicht überstehen. Ich konnte es nicht glauben. Als ich es nach Albany im Bundesstaat New York geschafft hatte, innerhalb von 24 Stunden, starb er. Das war einer der schwersten Momente meines Lebens und es ist immer noch schwer, so ziemlich jeden Tag."
Vertrauen schaffen in der Kirche
34 Jahre hatte Shakir Cannon mit der Sichelzellkrankheit gelebt. Michael Friend hatte gehofft, dass sein Freund und Partner zu den ersten gehören würde, die von der neuen Gentherapie profitieren. Dafür ging die Entwicklung nicht schnell genug. Seit dem plötzlichen Tod seines Mitstreiters kämpft Michael Friend umso intensiver alleine weiter. Er will vor allem bei Afroamerikanern Vertrauen aufbauen für Gentherapien. Der Weg dahin führt an einen überraschenden Ort: in die Kirche.
"Die schwarzen Kirchen, die Kirchen der Afroamerikaner waren immer die vertrauensvollste Institution in unserer Community. Die Menschen vertrauen den Führern der Kirche und vertrauen den Informationen, die sie dort bekommen. Deshalb ist es sehr wichtig, diese Diskussionen dort zuerst zu führen. Und man kann skalieren von fünf Kirchen zu 15.000. Das hängt nur davon ab, was man für Kapazitäten hat."
Viele Kirchen haben schon Gesundheitsprogramme. Sie könnten in Zukunft auch über Gentherapien informieren.
"Wir arbeiten dabei mit wissenschaftlichen Beratern. Afroamerikanischen Wissenschaftlern, die mit der Technik und Genomik sehr vertraut sind. Wir bringen die beiden Gruppen an einen Tisch."
Das klingt nach einer klugen Herangehensweise, nach einer, die auf die spezifischen Gegebenheiten der Community eingeht. Aber Michael Friend ist vielleicht etwas überengagiert. Er ist seiner Sache so verbunden, dass er, so sagt er, in den vergangenen zehn Jahren viel dafür aufgegeben und verloren hat: Freundschaften, Häuser, Autos. Dabei wird es gut noch einmal zehn, fünfzehn Jahre dauern, bis tatsächlich mehr als ein paar Dutzend Probanden von CRISPR profitieren können. Viele Fragen sind offen. Die klinischen Studien haben noch nicht begonnen und werden noch lange nicht abgeschlossen sein. Und CRISPR wäre eben nicht die einzige Option. Yetunde Olagbaju jedenfalls ist acht Jahre später glücklich mit der Knochenmarkspende ihres Bruders.
"Ich kann jetzt schwimmen gehen. Vorher konnte das eine Schmerzkrise auslösen, weil das kalte Wasser ein Schock für das System ist und der Körper darauf mit einer Schmerzkrise reagiert. Also, vorher konnte ich nicht schwimmen. Jetzt, dieses Jahr, lerne ich schwimmen. Ja, mein Leben hat sich sehr verändert. Ich muss mir jetzt auch keine Sorgen ums Kinderkriegen mehr machen. Viele schwangere Sichelzellpatienten verlieren entweder ihre Babys oder ihr Leben, weil das extra Stress für ihren Körper ist. Die Sorgen muss ich mir jetzt nicht mehr machen und ich bin bereit zu heiraten und Kinder zu kriegen."
Ihr Arzt, Robert Brodsky, sieht die CRISPR-Therapien kritisch. Er sagt aber auch, dass man ihnen eine Chance geben muss. Denn ohne Risiko ist seine Behandlungsmethode auch nicht.
"Knochenmarktransplantationen sind eine große Prozedur, die Risiken hat. Wir haben die Sterblichkeitsrate auf unter fünf Prozent bekommen, aber sie ist nicht null."
"Die schwarzen Kirchen, die Kirchen der Afroamerikaner waren immer die vertrauensvollste Institution in unserer Community. Die Menschen vertrauen den Führern der Kirche und vertrauen den Informationen, die sie dort bekommen. Deshalb ist es sehr wichtig, diese Diskussionen dort zuerst zu führen. Und man kann skalieren von fünf Kirchen zu 15.000. Das hängt nur davon ab, was man für Kapazitäten hat."
Viele Kirchen haben schon Gesundheitsprogramme. Sie könnten in Zukunft auch über Gentherapien informieren.
"Wir arbeiten dabei mit wissenschaftlichen Beratern. Afroamerikanischen Wissenschaftlern, die mit der Technik und Genomik sehr vertraut sind. Wir bringen die beiden Gruppen an einen Tisch."
Das klingt nach einer klugen Herangehensweise, nach einer, die auf die spezifischen Gegebenheiten der Community eingeht. Aber Michael Friend ist vielleicht etwas überengagiert. Er ist seiner Sache so verbunden, dass er, so sagt er, in den vergangenen zehn Jahren viel dafür aufgegeben und verloren hat: Freundschaften, Häuser, Autos. Dabei wird es gut noch einmal zehn, fünfzehn Jahre dauern, bis tatsächlich mehr als ein paar Dutzend Probanden von CRISPR profitieren können. Viele Fragen sind offen. Die klinischen Studien haben noch nicht begonnen und werden noch lange nicht abgeschlossen sein. Und CRISPR wäre eben nicht die einzige Option. Yetunde Olagbaju jedenfalls ist acht Jahre später glücklich mit der Knochenmarkspende ihres Bruders.
"Ich kann jetzt schwimmen gehen. Vorher konnte das eine Schmerzkrise auslösen, weil das kalte Wasser ein Schock für das System ist und der Körper darauf mit einer Schmerzkrise reagiert. Also, vorher konnte ich nicht schwimmen. Jetzt, dieses Jahr, lerne ich schwimmen. Ja, mein Leben hat sich sehr verändert. Ich muss mir jetzt auch keine Sorgen ums Kinderkriegen mehr machen. Viele schwangere Sichelzellpatienten verlieren entweder ihre Babys oder ihr Leben, weil das extra Stress für ihren Körper ist. Die Sorgen muss ich mir jetzt nicht mehr machen und ich bin bereit zu heiraten und Kinder zu kriegen."
Ihr Arzt, Robert Brodsky, sieht die CRISPR-Therapien kritisch. Er sagt aber auch, dass man ihnen eine Chance geben muss. Denn ohne Risiko ist seine Behandlungsmethode auch nicht.
"Knochenmarktransplantationen sind eine große Prozedur, die Risiken hat. Wir haben die Sterblichkeitsrate auf unter fünf Prozent bekommen, aber sie ist nicht null."
Langfristig die bessere Variante
Die Stammzelltransplantation mit CRISPR scheint zudem perspektivisch besser zu sein. Auf die heftige Chemotherapie, die heute bei beiden Therapieformen die defekten Stammzellen ausschaltet, kann möglicherweise verzichtet werden, solange das Immunsystem des Patienten noch formbar ist.
"Ich kann mir vorstellen, dass wir die Diagnose einmal vorgeburtlich machen werden. Da könnten wir die Mutation korrigieren, bevor das Kind geboren ist oder kurz danach. Dann bräuchten wir keine Chemotherapie, sondern könnten vielleicht Antikörper im Immunsystem nutzen, um die kranken Stammzellen sicher zu eliminieren und sie mit korrigierten, gesunden Stammzellen zu ersetzen. Da geht es hin, zu einer sichereren Behandlung, hoffentlich früher im Leben, bevor sie die Komplikationen der Sichelzell-Krankheit erfahren haben. Also, da geht es hin, aber da können wir nicht anfangen. Wir müssen erst mehr darüber lernen."
Für Mark Walters ist es nur folgerichtig, unter all den Erbkrankheiten die Sichelzellkrankheit als erste mit CRISPR heilen zu wollen. Es ist schließlich die älteste beschriebene Krankheit, die auf einer Genmutation beruht.
Diesmal sind Afroamerikaner diejenigen, die als erste profitieren sollen. Gleichzeitig sind sie aber wieder einmal diejenigen, die den Kopf hinhalten für all die anderen Kranken, die auf Heilung hoffen.
"Wenn wir mal an all die anderen Erbkrankheiten denken, die sich durch Genmanipulation heilen lassen könnten, also die von einer einzigen Mutation oder einem einzigen Gen verursacht werden, dann betrifft das 350 Millionen Menschen weltweit, die eine solche Krankheit haben. Aber die verteilen sich auf 7000 Krankheiten. Eine riesige Zahl. Und da begeistern sich Leute für CRISPR, weil man nur das Ziel anders wählen muss. Wir arbeiten daran, dass man das sehr schnell machen kann. Sodass man nicht jedes Mal, wenn man ein anderes Gen bearbeiten will, 100 Millionen Dollar investieren muss. Wir wollen Wege finden, die es Ärzten erlauben, sehr personalisierte Behandlungen anzubieten."
Jacob Corn ist Ende 2018 an die ETH Zürich umgezogen, kooperiert aber weiter mit Mark Walters in Kalifornien. Auch in Regensburg und Tübingen werden Sichelzell-Patienten rekrutiert. Wenn die Therapie funktioniert und zum Erfolg wird, könnten Millionen Menschen davon profitieren - zuerst Afroamerikaner und Patienten in Europa, dann Betroffene in Afrika und anderen Erdteilen. Und schließlich die Träger anderer Erbkrankheiten weltweit. Doch wenn sich die Risiken als größer herausstellen als erwartet, dann könnten die Gräben wieder tiefer werden. Denn ohne Zweifel lasten die Risiken für den medizinischen Fortschritt einmal mehr auf den Schultern der Afroamerikaner.
Für Mark Walters ist es nur folgerichtig, unter all den Erbkrankheiten die Sichelzellkrankheit als erste mit CRISPR heilen zu wollen. Es ist schließlich die älteste beschriebene Krankheit, die auf einer Genmutation beruht.
Diesmal sind Afroamerikaner diejenigen, die als erste profitieren sollen. Gleichzeitig sind sie aber wieder einmal diejenigen, die den Kopf hinhalten für all die anderen Kranken, die auf Heilung hoffen.
"Wenn wir mal an all die anderen Erbkrankheiten denken, die sich durch Genmanipulation heilen lassen könnten, also die von einer einzigen Mutation oder einem einzigen Gen verursacht werden, dann betrifft das 350 Millionen Menschen weltweit, die eine solche Krankheit haben. Aber die verteilen sich auf 7000 Krankheiten. Eine riesige Zahl. Und da begeistern sich Leute für CRISPR, weil man nur das Ziel anders wählen muss. Wir arbeiten daran, dass man das sehr schnell machen kann. Sodass man nicht jedes Mal, wenn man ein anderes Gen bearbeiten will, 100 Millionen Dollar investieren muss. Wir wollen Wege finden, die es Ärzten erlauben, sehr personalisierte Behandlungen anzubieten."
Jacob Corn ist Ende 2018 an die ETH Zürich umgezogen, kooperiert aber weiter mit Mark Walters in Kalifornien. Auch in Regensburg und Tübingen werden Sichelzell-Patienten rekrutiert. Wenn die Therapie funktioniert und zum Erfolg wird, könnten Millionen Menschen davon profitieren - zuerst Afroamerikaner und Patienten in Europa, dann Betroffene in Afrika und anderen Erdteilen. Und schließlich die Träger anderer Erbkrankheiten weltweit. Doch wenn sich die Risiken als größer herausstellen als erwartet, dann könnten die Gräben wieder tiefer werden. Denn ohne Zweifel lasten die Risiken für den medizinischen Fortschritt einmal mehr auf den Schultern der Afroamerikaner.