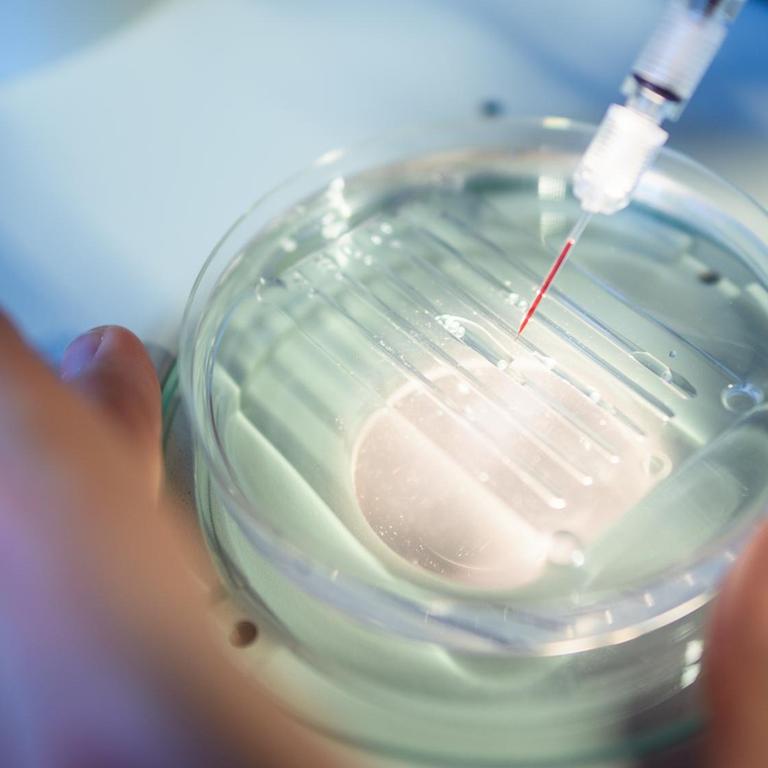
Am 23. November 1969, wenige Monate nach der ersten Mondlandung, begann unbemerkt von den meisten Menschen ein neues Zeitalter der Biologie. Wissenschaftler der Harvard-University hatten erstmals eine einzelne Erbanlange, ein Gen eines Bakteriums isoliert. Damit war es prinzipiell möglich, Gene von einem Individuum auf ein anderes zu übertragen. Es war das Startsignal für die Gentechnik, die drei Jahre später den ersten gentechnisch erzeugten Organismus hervorbrachte.
"Das ist für mich der eigentliche Umschlagspunkt. Also da hat qualitativ etwas Neues angefangen."
"Das ist für mich der eigentliche Umschlagspunkt. Also da hat qualitativ etwas Neues angefangen."
Hans-Jörg Rheinberger erforscht als Wissenschaftshistoriker die Ursprünge der Genforschung. Für den ehemaligen Direktor des Max-Planck-Instituts für Wissenschaftsgeschichte in Berlin waren 1969 und die folgenden drei Jahre entscheidend für die Zukunft der Menschheit. Denn durch die neue Gentechnik wurde es erstmals möglich, Eigenschaften oder Fähigkeiten von einer Art auf eine andere zu übertragen.
"Jetzt ist die Biologie in eine synthetische und konstruktive Phase eingetreten. Wir können nicht mehr nur analysieren, wir können konstruieren. Wir können Lebewesen nicht nur untersuchen, wir können sie auch dauerhaft verändern."
1969 wussten Genetiker bereits, wie das Erbmolekül DNA aufgebaut ist – als Doppelhelix: Zwei Stränge, die sich um einander winden. In den sechziger Jahren hatten sie herausgefunden, wie die DNA Informationen speichert. Sie kannten die chemischen Bausteine: Adenin, Thymin, Guanin und Cytosin und wussten, wie der biologische Code funktioniert.
"Jetzt ist die Biologie in eine synthetische und konstruktive Phase eingetreten. Wir können nicht mehr nur analysieren, wir können konstruieren. Wir können Lebewesen nicht nur untersuchen, wir können sie auch dauerhaft verändern."
1969 wussten Genetiker bereits, wie das Erbmolekül DNA aufgebaut ist – als Doppelhelix: Zwei Stränge, die sich um einander winden. In den sechziger Jahren hatten sie herausgefunden, wie die DNA Informationen speichert. Sie kannten die chemischen Bausteine: Adenin, Thymin, Guanin und Cytosin und wussten, wie der biologische Code funktioniert.
Als der Biologe Jon Beckwith, der Leiter der verantwortlichen Arbeitsgruppe an der Harvard-University, erstmals ein Gen isoliert hatte, war er 33 Jahre alt. Er galt nicht als Draufgänger, eher ein nachdenklicher Typ. Später schrieb er in einem Buch:
"Wir wussten bereits, dass Genmanipulationen Gefahren für die Menschheit bedeuten und fragten uns: Wer würde entscheiden, welche Gene verändert werden dürfen und wie lässt sich die Anwendung der genetischen Manipulation beim Menschen kontrollieren?"
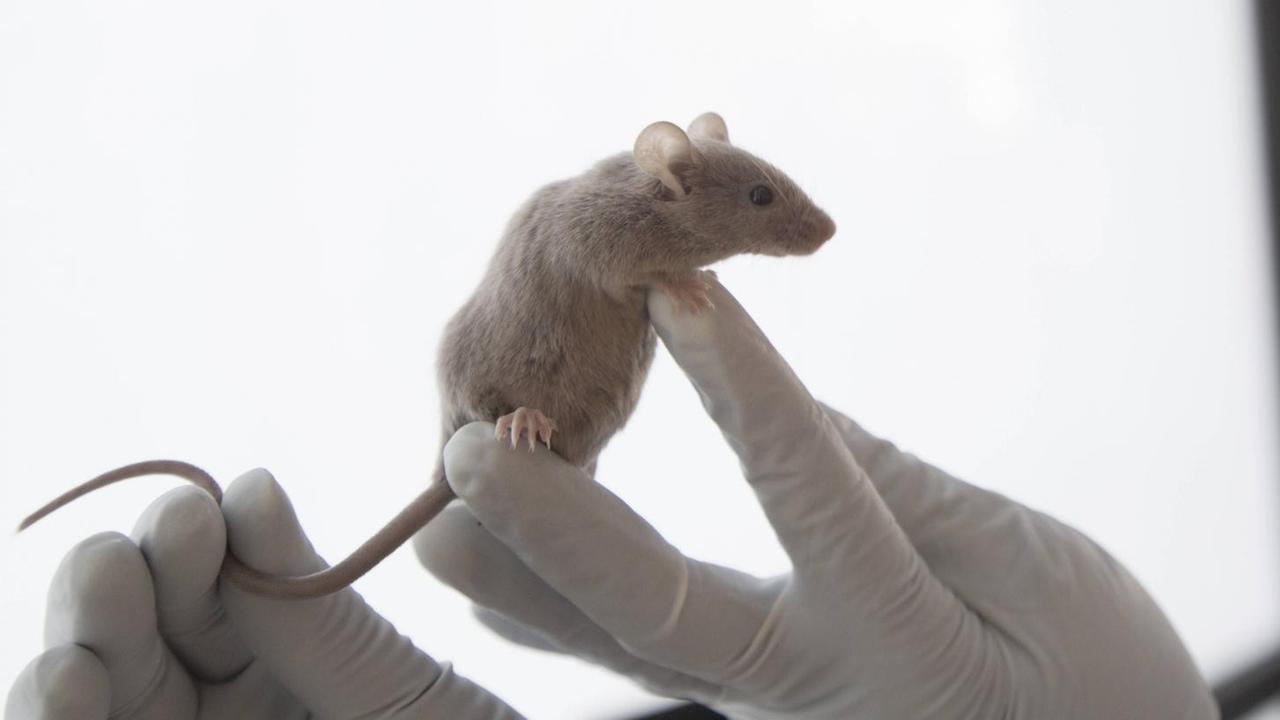
Die Grundlagen waren gelegt. Die Gentechnik kam schnell voran. 1973 entstand das erste gentechnisch veränderte Bakterium. Es gehörte zur Art Escherichia coli. 1974 folgte eine genmanipulierte Maus. Das erste transgene Säugetier.
"Ich denke, es war eine sehr interessante Zeit, wo man begann zu verstehen, wie Gene funktionieren, dass man Gene in Zellen hineinbringen kann, dass die aktiv sind."

Experimente an Bakterien und Mäusen
Es war der aus Deutschland stammende Genforscher Rudolf Jaenisch, der an der Universität von Philadelphia als erster das Erbmaterial einer Maus veränderte.
"Man konnte demnach ein Tier im ganz frühen Stadium von ein, zwei bis Vierzellstadium manipulieren. Und auf diese Weise haben wir die ersten transgenen Mäuse gemacht, was ich damals nicht wusste, denn den Begriff gab es ja noch nicht."
Die rasante Entwicklung wurde den Pionieren bald unheimlich. Sie diskutierten über ein Moratorium, einen vorübergehenden Forschungsstopp. 1975 trafen sich Genforscher mit Philosophen, Soziologen und Theologen in einer Kleinstadt an der kalifornischen Pazifikküste. Dort in Asilomar definierten sie die Grenzen der Gentechnik. Mehrheitlich sprachen sich die dort Versammelten gegen die Freisetzung manipulierter Bakterien aus - und gegen die Manipulation von Krankheitserregern. Die Gentechniker wollten sich vorsichtig in das neue Forschungsgebiet vortasten, so der Wissenschaftshistoriker Hans-Jörg Rheinberger.
"Die Frage stellt sich dann nur: Sollen wir das mit dem Menschen auch so machen, wie wir das mit Bakterien machen? Und da bekommt die Frage dann natürlich eine ethische Dimension, die man sich eben beim Umgang mit Bakterien in dieser Form nicht stellt."
In Asilomar bestand Konsens: Der Mensch sollte außen vorbleiben. Vorerst. Dennoch war den Pionieren klar: Nichts war mehr so wie zuvor.
"Das sind schon tolle Sachen. Und ich meine, man muss sich, denke ich mir, auch als Gesellschaft daran gewöhnen, dass es dem Leben jetzt an den Kragen geht."
Bevor die Forscher über die Veränderung des Menschen nachdachten, wandte man sich den Pflanzen zu. Auch sie konnte man zu Beginn der 1980er Jahre gentechnisch verändern. Die gesellschaftliche Debatte verließ die akademischen Zirkel und erreichte die Straße.
"Man konnte demnach ein Tier im ganz frühen Stadium von ein, zwei bis Vierzellstadium manipulieren. Und auf diese Weise haben wir die ersten transgenen Mäuse gemacht, was ich damals nicht wusste, denn den Begriff gab es ja noch nicht."
Die rasante Entwicklung wurde den Pionieren bald unheimlich. Sie diskutierten über ein Moratorium, einen vorübergehenden Forschungsstopp. 1975 trafen sich Genforscher mit Philosophen, Soziologen und Theologen in einer Kleinstadt an der kalifornischen Pazifikküste. Dort in Asilomar definierten sie die Grenzen der Gentechnik. Mehrheitlich sprachen sich die dort Versammelten gegen die Freisetzung manipulierter Bakterien aus - und gegen die Manipulation von Krankheitserregern. Die Gentechniker wollten sich vorsichtig in das neue Forschungsgebiet vortasten, so der Wissenschaftshistoriker Hans-Jörg Rheinberger.
"Die Frage stellt sich dann nur: Sollen wir das mit dem Menschen auch so machen, wie wir das mit Bakterien machen? Und da bekommt die Frage dann natürlich eine ethische Dimension, die man sich eben beim Umgang mit Bakterien in dieser Form nicht stellt."
In Asilomar bestand Konsens: Der Mensch sollte außen vorbleiben. Vorerst. Dennoch war den Pionieren klar: Nichts war mehr so wie zuvor.
"Das sind schon tolle Sachen. Und ich meine, man muss sich, denke ich mir, auch als Gesellschaft daran gewöhnen, dass es dem Leben jetzt an den Kragen geht."
Bevor die Forscher über die Veränderung des Menschen nachdachten, wandte man sich den Pflanzen zu. Auch sie konnte man zu Beginn der 1980er Jahre gentechnisch verändern. Die gesellschaftliche Debatte verließ die akademischen Zirkel und erreichte die Straße.
Genexperimente am Kölner Stadtrand
Das Max-Planck-Institut für Züchtungsforschung in Köln war eines der führenden Forschungszentren auf seinem Gebiet. Nachdem in vielen anderen Ländern Freisetzungsversuche stattgefunden hatten, wollten die Kölner Forscher ebenfalls im Freiland experimentieren.
Zur Grundlagenforschung sollten im Frühjahr 1990 genveränderte Petunien am Stadtrand von Köln ausgesät werden. Schon bald kam es zu Protesten gegen die Gentechnik, erinnert sich Joachim Spangenberg. Der Kölner Biologe und Ökonom arbeitet für das europäische Forschungsinstitut SETI. 1990 war er bei den Protestierern.
"Das war eine Zeit, wo sehr viele öffentliche Diskussionen über die potentiellen Risiken der Gentechnik liefen, und ein zunehmendes Misstrauen zwischen Wissenschaft und Gesellschaft aufkam. Und dann wurde direkt vor meiner Haustür das erste Freisetzungsexperiment beschlossen."
Zur Grundlagenforschung sollten im Frühjahr 1990 genveränderte Petunien am Stadtrand von Köln ausgesät werden. Schon bald kam es zu Protesten gegen die Gentechnik, erinnert sich Joachim Spangenberg. Der Kölner Biologe und Ökonom arbeitet für das europäische Forschungsinstitut SETI. 1990 war er bei den Protestierern.
"Das war eine Zeit, wo sehr viele öffentliche Diskussionen über die potentiellen Risiken der Gentechnik liefen, und ein zunehmendes Misstrauen zwischen Wissenschaft und Gesellschaft aufkam. Und dann wurde direkt vor meiner Haustür das erste Freisetzungsexperiment beschlossen."

Proteste, Sitzblockaden, Brandbomben
Wochenlang blockierten Hunderte Gentechnik-Gegner das Kölner Max-Planck-Institut und verhinderten die Aussaat der Petunien.
"Ich habe das damals immer so empfunden, ähnlich wie eine Sitzblockade vor einem Militärlager. Es ist illegal, man muss mit den Konsequenzen leben, aber es tut keinem weh. Es hat aber ein paar Idioten gegeben, die Drohungen gemacht haben, und einmal ist sogar, glaube ich, eine Brandbombe in den Keller des MPI geworfen worden."
Auf der anderen Seite des Tors stand Heinz Saedler, 1990 einer der führenden Wissenschaftler des Instituts.
"Das war hier vor Ort schon aufgeheizt. Das ist keine Frage. Aber es war nicht so, dass das den Betrieb gestört hätte. Soweit ging es nicht. Also die Polizei wollte viel drastischere Maßnahmen ergreifen. Die haben wir unterbunden. Da haben wir gesagt: Das wollen wir nicht. Wir wollen keinen Krieg daraus machen."
"Ich habe das damals immer so empfunden, ähnlich wie eine Sitzblockade vor einem Militärlager. Es ist illegal, man muss mit den Konsequenzen leben, aber es tut keinem weh. Es hat aber ein paar Idioten gegeben, die Drohungen gemacht haben, und einmal ist sogar, glaube ich, eine Brandbombe in den Keller des MPI geworfen worden."
Auf der anderen Seite des Tors stand Heinz Saedler, 1990 einer der führenden Wissenschaftler des Instituts.
"Das war hier vor Ort schon aufgeheizt. Das ist keine Frage. Aber es war nicht so, dass das den Betrieb gestört hätte. Soweit ging es nicht. Also die Polizei wollte viel drastischere Maßnahmen ergreifen. Die haben wir unterbunden. Da haben wir gesagt: Das wollen wir nicht. Wir wollen keinen Krieg daraus machen."
Die Kölner Forscher konnten schließlich über 30.000 Petunien aussähen. Die Ergebnisse ihrer Studie überraschten sie. Die Farben der Blüten verteilten sich anders als erwartet. Die Gentechnik-Gegner sahen sich bestätigt. Ihrer Meinung nach zeigten die Ergebnisse, wie unberechenbar die neue Technik ist. Unter Wissenschaftlern galt diese Studie später als Nachweis des Zusammenwirkens von Umwelt und Genetik. Viel wichtiger als die wissenschaftlichen Folgen waren die Auswirkungen für die Beziehung zwischen Wissenschaft und Öffentlichkeit, erläutert Joachim Spangenberg. Er steht der Genforschung nach wie vor kritisch gegenüber.
"Und das hat bei den Wissenschaftlern – zumindest meiner Beobachtung nach - zu einer ziemlichen Paranoia geführt, die also dazu führte, dass Diskussionen abgebrochen wurden. Eine völlige Verhärtung der Positionen. Die fühlten sich im Belagerungszustand und waren nur noch auf Verteidigung aus. Und das ist eine sehr schlechte Grundlage für einen Dialog."
Die Atmosphäre blieb jahrzehntelang vergiftet und wurde geprägt durch Misstrauen auf beiden Seiten. Genforscher wie Heinz Saedler fühlen sich von der Öffentlichkeit missverstanden.
"Die Leute haben Ängste, obwohl es weltweit keinen Fall gibt, der darauf hindeutet, dass der Anbau gentechnisch veränderter Pflanzen ein großes Risiko darstellt, oder überhaupt ein Risiko darstellt."

Bis heute ein umstrittenes Forschungsgebiet
Ob Gefahren von der Gentechnik ausgehen, wurde vielfach untersucht. Aber es blieb dabei: In der Interpretation des vorhandenen Wissens unterscheiden sich Gentechnik-Gegner und Befürworter auch Jahrzehnte später. Unstrittig ist: Freigesetzte Gene lassen sich nicht mehr einfangen. Sie können von einer Art auf die andere übertragen werden. Joachim Spangenberg:
"Inzwischen gibt es den Nachweis, dass Gene ausgekreuzt werden können in andere Nutzpflanzenarten, aber auch in Schädlingsarten. Wir haben in zahlreichen Bereichen inzwischen die Bestätigung, dass die Schädlingsresistenz-Gene in Unkräuter übergegangen sind und jetzt mit erhöhten Spritzmengen versucht wird muss dagegen anzugehen."
1994 kam in den USA die genetisch veränderte, so genannte Anti-Matsch-Tomate auf den Markt. Sie sollte auch bei längerer Lagerung frisch und schmackhaft bleiben. Überzeugen konnte sie nicht. 1997 verschwand die genveränderte Tomate wieder aus den Supermärkten. Über Gesundheitsschäden durch genveränderte Lebensmittel wurde seitdem immer wieder diskutiert. Allgemein anerkannte Beweise gibt es nicht.
"Inzwischen gibt es den Nachweis, dass Gene ausgekreuzt werden können in andere Nutzpflanzenarten, aber auch in Schädlingsarten. Wir haben in zahlreichen Bereichen inzwischen die Bestätigung, dass die Schädlingsresistenz-Gene in Unkräuter übergegangen sind und jetzt mit erhöhten Spritzmengen versucht wird muss dagegen anzugehen."
1994 kam in den USA die genetisch veränderte, so genannte Anti-Matsch-Tomate auf den Markt. Sie sollte auch bei längerer Lagerung frisch und schmackhaft bleiben. Überzeugen konnte sie nicht. 1997 verschwand die genveränderte Tomate wieder aus den Supermärkten. Über Gesundheitsschäden durch genveränderte Lebensmittel wurde seitdem immer wieder diskutiert. Allgemein anerkannte Beweise gibt es nicht.

Skepsis gegenüber grüner Gentechnik hält vor allem in Europa an
In Europa blieb die Skepsis gegenüber der so genannten "Grünen Gentechnik" groß. Das änderte jedoch nichts an ihrer weltweiten Verbreitung. Hauptsächlich Baumwolle, Soja und Mais wachsen seit den 1990er Jahren in den USA, Südamerika, China, Indien und vielen anderen Ländern. Die meisten dieser Pflanzen besitzen eine Resistenz gegen Unkrautvernichtungsmittel. Das erleichtert den Einsatz so genannter Totalherbizide und schädigt so indirekt die Natur – insbesondere Wildpflanzen, Insekten und Vögel.
Ganz anders verlief die Debatte um den Einsatz der Gentechnik in der Medizin. Sie war von Anfang an mit Hoffnungen verbunden.
1990 wurden in den USA erstmals Körperzellen eines Menschen gentechnisch verändert. Ein vierjähriges Mädchen litt an einer vererbten Immunschwäche und erhielt mehrere Genspritzen. Langsam verbesserte sich ihr Zustand. Ob die Gentherapie einen Anteil daran hatte, blieb unklar. Denn das Mädchen erhielt außerdem Enzyme, um ihr Immunsystem aufzubauen. Es folgten Hunderte weitere Studien. Die meisten erfolglos. Es dauerte 12 Jahre bis erste Erfolge zu verzeichnen waren, so Toni Cathomen, Professor für Gentherapie an der Universität Freiburg.
"Die erste erfolgreiche Gentherapie-Studie war tatsächlich 2002 publiziert worden von den Kollegen in Frankreich, in Paris. Und das war die Gentherapie-Studie bei Kindern, die an schweren vererbten Immundefekten erkrankt sind. Das war das erste Mal, dass man in der Klinik zeigen konnte, dass die Gentherapie einen therapeutischen Effekt erzielt."
Ganz anders verlief die Debatte um den Einsatz der Gentechnik in der Medizin. Sie war von Anfang an mit Hoffnungen verbunden.
1990 wurden in den USA erstmals Körperzellen eines Menschen gentechnisch verändert. Ein vierjähriges Mädchen litt an einer vererbten Immunschwäche und erhielt mehrere Genspritzen. Langsam verbesserte sich ihr Zustand. Ob die Gentherapie einen Anteil daran hatte, blieb unklar. Denn das Mädchen erhielt außerdem Enzyme, um ihr Immunsystem aufzubauen. Es folgten Hunderte weitere Studien. Die meisten erfolglos. Es dauerte 12 Jahre bis erste Erfolge zu verzeichnen waren, so Toni Cathomen, Professor für Gentherapie an der Universität Freiburg.
"Die erste erfolgreiche Gentherapie-Studie war tatsächlich 2002 publiziert worden von den Kollegen in Frankreich, in Paris. Und das war die Gentherapie-Studie bei Kindern, die an schweren vererbten Immundefekten erkrankt sind. Das war das erste Mal, dass man in der Klinik zeigen konnte, dass die Gentherapie einen therapeutischen Effekt erzielt."
Einige seltene Krankheiten konnten in den folgenden Jahren mit Hilfe einer Gentherapie geheilt oder wenigstens gut behandelt werden, so dass Patienten davon profitierten.
2012 sorgte ein neues gentechnologisches Werkzeug erneut für Optimismus unter den Genforschern: Die so genannte Genschere, bekannt auch unter dem wissenschaftlichen Kürzel Crispr/Cas 9. Ein Biomolekül, mit dem sich Bakterien gegen Viren wehren. Toni Cathomen:
"Also, man muss da wirklich von einer Crispr-Revolution sprechen, weil sich diese Technologie so schnell verbreitet hat, dass eigentlich jedes Labor heutzutage die einsetzen kann und auch genetische Veränderungen in ganz verschiedenen Organismen auch herbeiführen kann."
"Crispr/Cas9 besitzt einen spezifischen Mechanismus, um DNA zu erkennen – und der ist ziemlich gut."
Die französische Mikrobiologin Emmanuelle Charpentier erforschte den Abwehrmechanismus von Bakterien und fand schließlich gemeinsam mit der Amerikanerin Jennifer Doudna heraus, wie die Genschere arbeitet und wie sie sich programmieren lässt.
"Im Prinzip ist das sehr preiswert, einfach anzuwenden, hoch effizient und schnell. Deshalb ist es so verlockend für die Wissenschaft."
2012 sorgte ein neues gentechnologisches Werkzeug erneut für Optimismus unter den Genforschern: Die so genannte Genschere, bekannt auch unter dem wissenschaftlichen Kürzel Crispr/Cas 9. Ein Biomolekül, mit dem sich Bakterien gegen Viren wehren. Toni Cathomen:
"Also, man muss da wirklich von einer Crispr-Revolution sprechen, weil sich diese Technologie so schnell verbreitet hat, dass eigentlich jedes Labor heutzutage die einsetzen kann und auch genetische Veränderungen in ganz verschiedenen Organismen auch herbeiführen kann."
"Crispr/Cas9 besitzt einen spezifischen Mechanismus, um DNA zu erkennen – und der ist ziemlich gut."
Die französische Mikrobiologin Emmanuelle Charpentier erforschte den Abwehrmechanismus von Bakterien und fand schließlich gemeinsam mit der Amerikanerin Jennifer Doudna heraus, wie die Genschere arbeitet und wie sie sich programmieren lässt.
"Im Prinzip ist das sehr preiswert, einfach anzuwenden, hoch effizient und schnell. Deshalb ist es so verlockend für die Wissenschaft."

Auch in der Pflanzenzüchtung fand die neue Genschere schnell Anwendung. In einem kleinen Gewächshaus nicht weit vom Labor an der Universität Münster wachsen ungewöhnliche Tomatenpflanzen. Die Früchte sind winzig klein, noch kleiner als die üblichen Cocktail-Tomaten. Sie stammen direkt von den wilden Vorfahren der Tomate ab, erläutert der Molekularbiologe Kai Edel.
"Wir sehen hier verschiedene Tomatenpflanzen. Das sind alles Solanum Pimpinellifolium, also Wildtomaten. Das sind zum einen die Tomaten unverändert, und dann unsere veränderten Tomaten mit den neuen Eigenschaften."
"Wir sehen hier verschiedene Tomatenpflanzen. Das sind alles Solanum Pimpinellifolium, also Wildtomaten. Das sind zum einen die Tomaten unverändert, und dann unsere veränderten Tomaten mit den neuen Eigenschaften."

Mehr Natur und gesündere Ernährung durch Gentechnik
Mit Hilfe der Genschere Crispr/Cas 9 haben die Molekularbiologen aus Münster die Wildtomaten so verändert, dass ihre Früchte größer wurden - und überhaupt essbar. Zugleich sind sie robuster, schmackhafter und gesünder als die üblichen Zuchttomaten im Supermarkt oder im Gemüseladen.
"Das Grundproblem ist im Grunde, dass die gezüchteten Tomaten, die über Jahrhunderte lang gezüchtet wurden, dass die an Erbgutinformation verloren haben. Die Vielfältigkeit des Erbguts hat deutlich abgenommen aufgrund des Züchtungsprozesses, der immer vor allem auf Ertrag zielte. Wir haben jetzt eine Wildtomate genommen und die im Grunde wieder zu einer Nutztomate gemacht, um die Eigenschaften der Wildtomate in die Nutztomate zu überführen."
Das Prinzip klingt überraschend: Mehr Natur und gesündere Ernährung durch Gentechnik. Mit Hilfe der neuen Genwerkzeuge können Pflanzen gezielter verändert werden. Das kann so schonend geschehen, dass sie sich nicht von konventionell gezüchteten Sorten unterscheiden. Die neuen Pflanzen können sogar umweltverträglicher sein als hochgezüchtete Exemplare ohne Gentechnik.
Viele Wissenschaftler wünschen sich deshalb, dass diese neuen Pflanzen nicht als gentechnisch manipuliert gekennzeichnet werden müssen. Denn dadurch hätten sie bei den Verbrauchern keine Chance. Sie wollen den Fokus auf die Produkte legen, nicht auf die Methode, mit der sie gezüchtet wurden. Dann müssten sie nicht gekennzeichnet werden.
Lilian Marx-Stölting von der Berlin Brandenburgischen Akademie der Wissenschaften arbeitet für den Gentechnologie-Bericht. Sie spricht sich für eine Kennzeichnung von Lebensmitteln aus, die mit Hilfe der neuen Genschere entstanden sind.
"Aus meiner Sicht ist das Gentechnik und zwar, weil für mich der Prozess entscheidend ist. Guckt man nur auf das Produkt, kann ich nachvollziehen, dass man sagt: Das ist doch dasselbe oder das gleiche, und das muss gleichbehandelt werden. Guckt man sich den Prozess an, ist es aber nicht das gleiche. Und ich halte es für wichtig im Sinne der Transparenz und für die Autonomie der Verbraucher, dass man hier ganz klar Gentechnik auch als solche benennt."
"Das Grundproblem ist im Grunde, dass die gezüchteten Tomaten, die über Jahrhunderte lang gezüchtet wurden, dass die an Erbgutinformation verloren haben. Die Vielfältigkeit des Erbguts hat deutlich abgenommen aufgrund des Züchtungsprozesses, der immer vor allem auf Ertrag zielte. Wir haben jetzt eine Wildtomate genommen und die im Grunde wieder zu einer Nutztomate gemacht, um die Eigenschaften der Wildtomate in die Nutztomate zu überführen."
Das Prinzip klingt überraschend: Mehr Natur und gesündere Ernährung durch Gentechnik. Mit Hilfe der neuen Genwerkzeuge können Pflanzen gezielter verändert werden. Das kann so schonend geschehen, dass sie sich nicht von konventionell gezüchteten Sorten unterscheiden. Die neuen Pflanzen können sogar umweltverträglicher sein als hochgezüchtete Exemplare ohne Gentechnik.
Viele Wissenschaftler wünschen sich deshalb, dass diese neuen Pflanzen nicht als gentechnisch manipuliert gekennzeichnet werden müssen. Denn dadurch hätten sie bei den Verbrauchern keine Chance. Sie wollen den Fokus auf die Produkte legen, nicht auf die Methode, mit der sie gezüchtet wurden. Dann müssten sie nicht gekennzeichnet werden.
Lilian Marx-Stölting von der Berlin Brandenburgischen Akademie der Wissenschaften arbeitet für den Gentechnologie-Bericht. Sie spricht sich für eine Kennzeichnung von Lebensmitteln aus, die mit Hilfe der neuen Genschere entstanden sind.
"Aus meiner Sicht ist das Gentechnik und zwar, weil für mich der Prozess entscheidend ist. Guckt man nur auf das Produkt, kann ich nachvollziehen, dass man sagt: Das ist doch dasselbe oder das gleiche, und das muss gleichbehandelt werden. Guckt man sich den Prozess an, ist es aber nicht das gleiche. Und ich halte es für wichtig im Sinne der Transparenz und für die Autonomie der Verbraucher, dass man hier ganz klar Gentechnik auch als solche benennt."
EuGH fordert Kennzeichnungspflicht für gentechnisch veränderte Pflanzen
Der Europäische Gerichtshof entschied 2018, dass Pflanzen, die mit Hilfe der Genschere Crispr/Cas9 entstanden sind, als Gentechnik gekennzeichnet werden müssen. Eine Ausnahme sei nicht möglich, da es nur wenig Erfahrung mit der neuen Technik gebe.

Diskussion um Genschere Crispr/Cas9
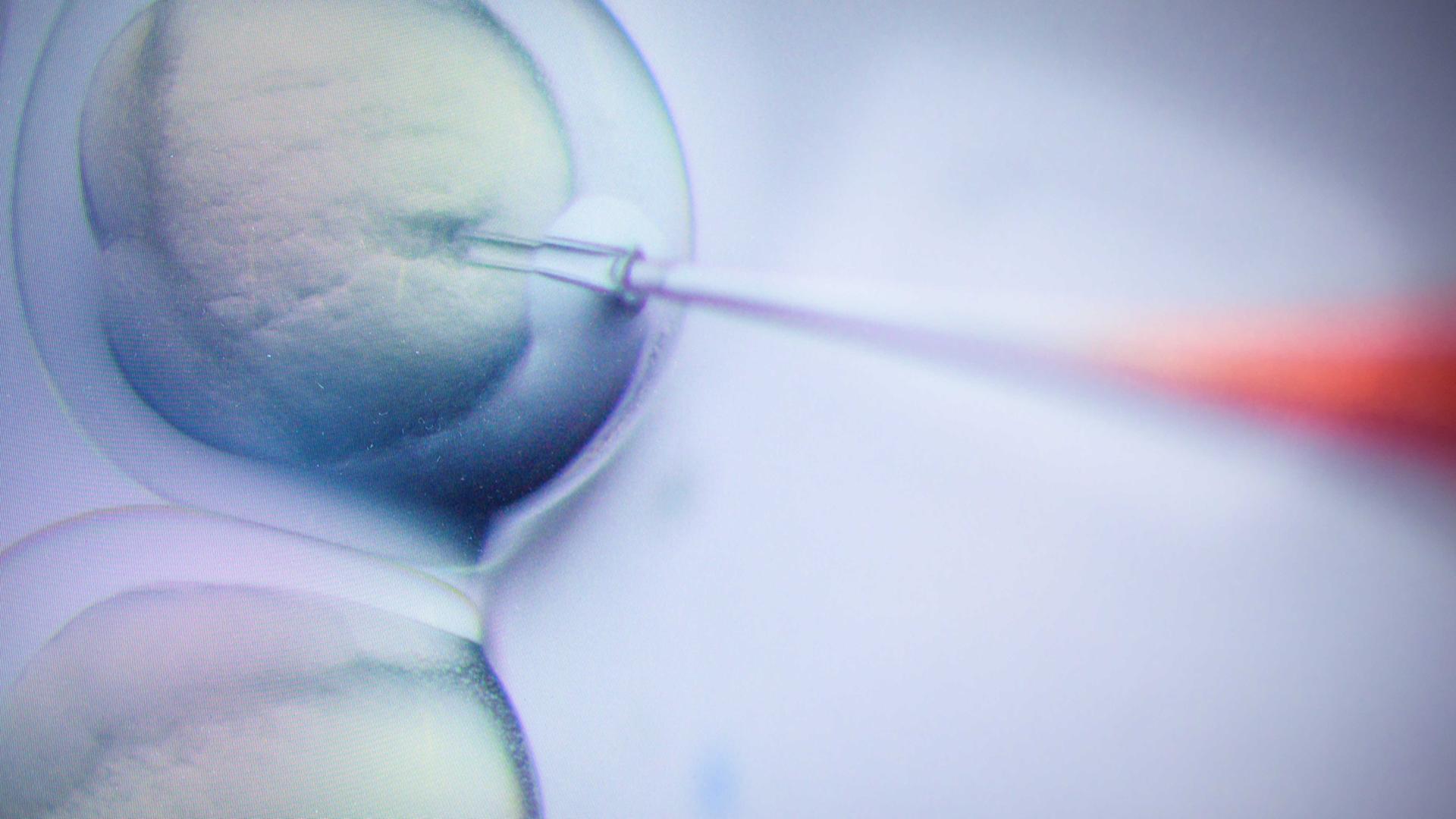
Auch in der Medizin gab es 2018 Diskussionsstoff. Denn die Genschere ermöglicht nicht nur die Veränderung von Körperzellen zu medizinischen Zwecken. Auch Embryonen, Eizellen oder Spermien können mit dem neuen Werkzeug verändert werden. Diese Veränderungen würden den ganzen Körper eines Menschen betreffen und an folgende Generationen weitergeben.
Während die Öffentlichkeit noch diskutierte, schuf ein chinesischer Wissenschaftler namens He Jiankui von der Universität Shenzhen Tatsachen. Er hatte Embryonen genetisch verändert und so ein genmanipuliertes Zwillingspärchen geschaffen. Seinen Durchbruch verkündete der Wissenschaftler nicht wie üblich in der Fachpresse, sondern in einem Video auf Youtube.
"Zwei schöne, kleine Mädchen mit Namen Lulu und Nana erblickten das Licht der Welt. Gesund und munter, wie jedes andere Baby."
Die Manipulation sollte die beiden Mädchen vor dem Aids-Erreger H.I.V. schützen, erklärte er. Es handelte sich um eine Genveränderung, die an folgende Generationen vererbt wird: Ein Eingriff in die Evolution oder in die Schöpfung. Damit wurde eine Grenze überschritten. He Jiankui erwartete Applaus oder wenigstens angeregte Diskussionen. Doch die Kollegen distanzierten sich von ihm. Auch Toni Cathomen von der Universität Freiburg.
"Was passiert eigentlich fünf Jahre nach Therapie, was passiert zehn Jahre nach Therapie? Und jetzt diesen großen Schritt zu machen und tatsächlich das in der Keimbahn, also im Embryo einzusetzen, ohne dass ich eigentlich eine Technologiefolgenabschätzung durchgeführt habe vorher, das ist einfach absolut unverantwortlich."
Nach dem öffentlichen Aufschrei wurde es wieder ruhig. Dabei geht es um eine Menschheitsfrage. Die Manipulation des Menschen, manche sprechen von Designer-Babys, ändert unser Menschenbild, so Christiane Woopen, Professorin für Ethik und Theorie der Medizin an der Universität zu Köln.
"Da geht es einfach darum, dass Menschen untereinander nicht darüber bestimmen sollten, wie die genetische Ausstattung eines Menschen gestaltet sein soll. Das heißt, dass wir uns einem Zufall verdanken, einer Zeugung, bei der eben in einem Zufallsprozess Gene zusammengefügt werden, damit wir nicht einander Danke sagen müssen, den Eltern dafür, dass sie uns diese oder jene Gene mitgegeben haben, oder ihnen vorwerfen, dass sie uns nicht verändert haben, weil wir doch viel bessere Eigenschaften hätten haben können."
Während die Öffentlichkeit noch diskutierte, schuf ein chinesischer Wissenschaftler namens He Jiankui von der Universität Shenzhen Tatsachen. Er hatte Embryonen genetisch verändert und so ein genmanipuliertes Zwillingspärchen geschaffen. Seinen Durchbruch verkündete der Wissenschaftler nicht wie üblich in der Fachpresse, sondern in einem Video auf Youtube.
"Zwei schöne, kleine Mädchen mit Namen Lulu und Nana erblickten das Licht der Welt. Gesund und munter, wie jedes andere Baby."
Die Manipulation sollte die beiden Mädchen vor dem Aids-Erreger H.I.V. schützen, erklärte er. Es handelte sich um eine Genveränderung, die an folgende Generationen vererbt wird: Ein Eingriff in die Evolution oder in die Schöpfung. Damit wurde eine Grenze überschritten. He Jiankui erwartete Applaus oder wenigstens angeregte Diskussionen. Doch die Kollegen distanzierten sich von ihm. Auch Toni Cathomen von der Universität Freiburg.
"Was passiert eigentlich fünf Jahre nach Therapie, was passiert zehn Jahre nach Therapie? Und jetzt diesen großen Schritt zu machen und tatsächlich das in der Keimbahn, also im Embryo einzusetzen, ohne dass ich eigentlich eine Technologiefolgenabschätzung durchgeführt habe vorher, das ist einfach absolut unverantwortlich."
Nach dem öffentlichen Aufschrei wurde es wieder ruhig. Dabei geht es um eine Menschheitsfrage. Die Manipulation des Menschen, manche sprechen von Designer-Babys, ändert unser Menschenbild, so Christiane Woopen, Professorin für Ethik und Theorie der Medizin an der Universität zu Köln.
"Da geht es einfach darum, dass Menschen untereinander nicht darüber bestimmen sollten, wie die genetische Ausstattung eines Menschen gestaltet sein soll. Das heißt, dass wir uns einem Zufall verdanken, einer Zeugung, bei der eben in einem Zufallsprozess Gene zusammengefügt werden, damit wir nicht einander Danke sagen müssen, den Eltern dafür, dass sie uns diese oder jene Gene mitgegeben haben, oder ihnen vorwerfen, dass sie uns nicht verändert haben, weil wir doch viel bessere Eigenschaften hätten haben können."

Viele offene Fragen
Es bestehen keine Zweifel mehr: Wie jedes andere Lebewesen lässt sich der Mensch gentechnisch verändern. Embryonenforschung in diesem Bereich findet in mehreren Staaten weltweit statt. Die Weltgesundheits-organisation WHO gründete eine Gruppe von Experten, die die Grenzen der Genforschung neu definieren soll. Eine verbindliche, internationale Ächtung der Genmanipulation am Menschen kam nicht zustande.